Planten en boeren, met hun drang 1: Fotosynthese, successie en bodem*
JAN VAN ARKEL

In dit artikel bespreek ik de natuurlijke gang van zaken bij planten en hoe de landbouw daarop inbreekt. Maar eerst benoem ik, bij wijze van ondergrond, nog even een paar nuttige begrippen. Ik grijp terug op het artikel ‘De natuur van de economie’ van Jane Jacobs in de rubriek Complexiteit (lees daar de uitgebreide versie). Zij stelt de vraag: ‘Waarom blijft eigenlijk niet alles zoals eerst?’ En zij beantwoordt die als volgt:
Dat komt door het verschijnsel ontwikkeling. Ontwikkeling kun je omschrijven als aanmerkelijke kwalitatieve verandering. Gewoonlijk komt die in kleine stapjes, al kan elke stap in een verandering van aard belangrijk zijn. We kunnen daarbij drie dingen onderscheiden.
Ten eerste: Differentiatie komt tevoorschijn uit algemeenheid. Ongeacht tempo, schaal, levend of niet, dit principe is overal van toepassing.
En ten tweede: Differentiaties worden algemeenheden waaruit vervolgens weer differentiaties tevoorschijn komen.
Ontwikkeling is met andere woorden een proces dat maar doorgaat, dat complexiteit en diversiteit creëert, omdat een vermenigvuldiging van algemeenheden de bron vormt voor een vermenigvuldiging van differentiaties. Soms gebeuren die gelijktijdig, soms volgt de ene op de andere. Als een eenvoudig basisprincipe levert dit proces, steeds weer herhaald en herhaald, een duizelingwekkende diversiteit op. (Zie ook de figuur in aflevering 8 van het eerste artikel ‘Waar komt de economische groei vandaan?’ in de rubriek Economie.)
Bij het woord ontwikkeling denk je misschien direct aan economische ontwikkeling, maar het is alom aan de gang, bijvoorbeeld ook in de evolutie. Uit de ongespecialiseerde ratachtige voeten van de vroege zoogdieren ontwikkelden zich zulke uiteenlopende vormen als paardenhoeven, vleermuisvleugels en walvisvinnen. Maar zo’n rechte ontwikkelingslijn klinkt wat al te gemakkelijk. Een paard heeft niet alleen voorouders nodig, maar ook gras; en gras vergt een bodem, en een bodem vergt niet alleen verwering maar ook een hele rijkdom aan bodemleven, met compostering en afbraak en al. En bij een walvis is dat alles weer heel anders. Daar hebben we het derde punt te pakken: Ontwikkeling steunt op co-ontwikkeling. Ontwikkeling zien als een lijn, of zelfs als een verzameling van lijnen die maar doorgaan en doorgaan, is niet bruikbaar. Ontwikkeling opereert als een web van co-ontwikkelingen die van elkaar afhankelijk zijn. Want zonder co-ontwikkelingsweb geen ontwikkeling.
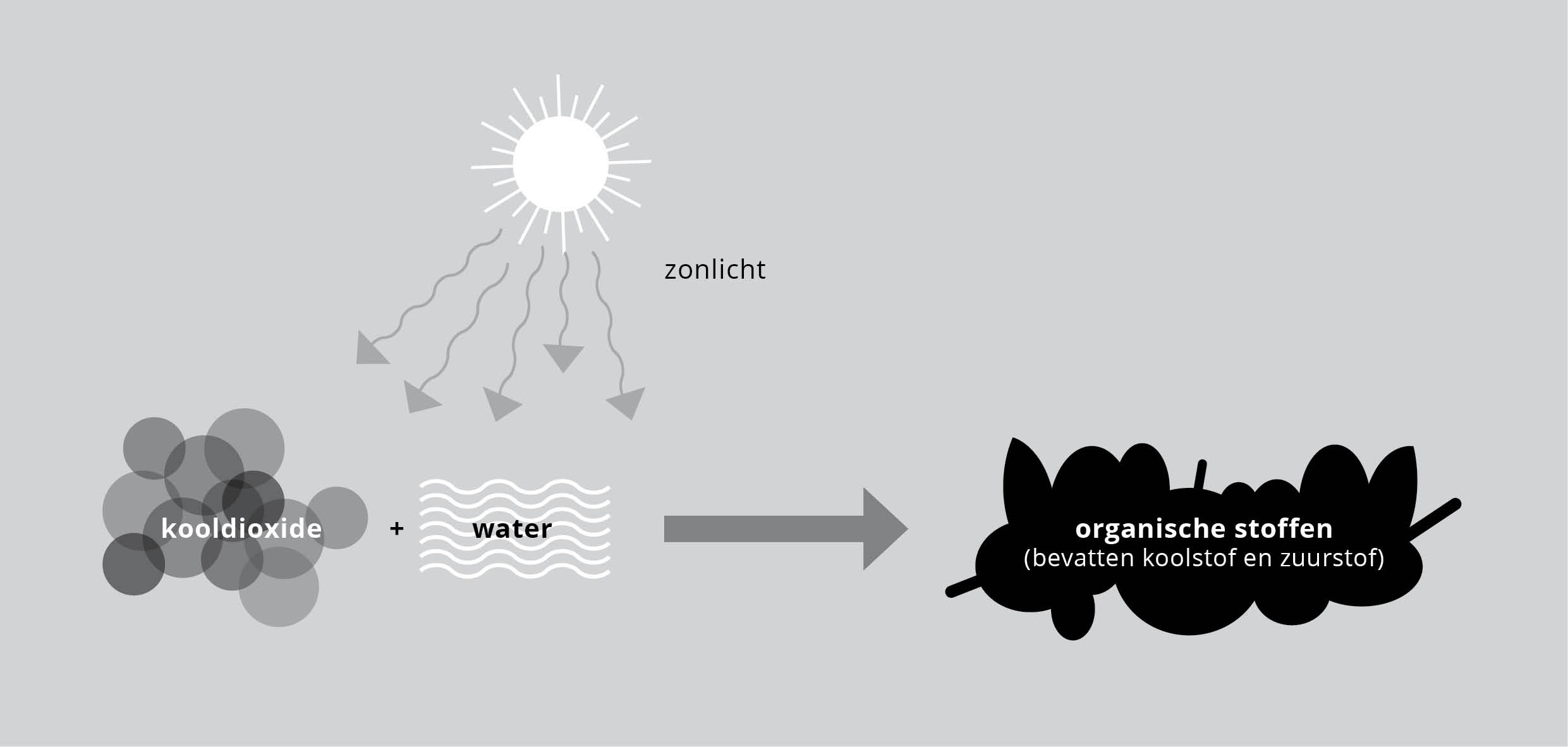
Figuur 1: Fotosynthese.
Zo kenden groene plantencellen een co-ontwikkeling met chloroplasten.* Deze symbiose maakt het mogelijk zonlicht te vangen en die vorm van energie te gebruiken om koolstof uit kooldioxide los te breken. Het afvalproduct zuurstof vervult dan weer onze behoefte om te ademen. Zo raakte het web van de co-evolutie in de loop van de tijd stap voor stap verfijnder. En zo is het met alle co-ontwikkelingswebben. We kunnen er gerust van uitgaan dat wederzijds invloedrijke co-ontwikkelingen net zo oud zijn als ontwikkeling zelf. We zijn daarom misschien al gauw geneigd het coöperatie te noemen, maar met die naam moet samenwerking ook doelbewust zijn. Omdat de wereld vol onbedoelde samenwerking is, kunnen we het volgens Jane Jacobs beter ‘onderlinge afhankelijkheid’ noemen.*
Jane Jacobs stelt dan bij het begrip evolutie nog de vraag: ‘Hoe verhoudt dit zich dat tot concurrentie, tot ‘het overleven van de best aangepaste’ van Darwin?’ En zij geeft direct zelf het antwoord: Die concurrentie bestaat natuurlijk, maar hij bestaat naast de onderlinge afhankelijkheid. Concurrentie om voedsel en voortplanting vindt plaats in een arena. In de natuur is de arena een habitat. De best aangepaste panter in de jungle kan het schudden als zijn habitat eraan gaat (om plaats te maken voor palmoliewinning). Het is net zo met de bij die geen honing vindt zonder bloemen. En wat is een habitat? Dat is een ingewikkeld, verfijnd web van onderlinge afhankelijkheden.
Behalve ‘ontwikkeling’ onderscheidt Jane Jacobs nog drie natuurlijke principes: ‘expansie’, ‘bijtanken’, en ‘zelfcorrectie’. We lopen ze kort langs, maar eerst hebben we het even over het begrip ecosysteem. Pas met aflevering vijf begint het eigenlijke artikel, zou je kunnen zeggen.

Ontwikkeling leidt in de natuur tot ecosystemen.* Figuur 2 toont een uiterst vereenvoudigd model van zo’n systeem. Je ziet hier 26 eenheden, in werkelijkheid zijn er miljoenen. Elke eenheid kan trouwens op zichzelf weer een compleet ecosysteem zijn, zoals een bodem, een meer, een gemeenschap van dieren, of de darmflora van een mens. De pijlen in de figuur geven de richting van iets aan, bijvoorbeeld een voedingselement, maar als puntje bij paaltje komt, tonen ze energiestromen, waarover straks meer. Op de stroom van energie na zijn rijpe ecosystemen in essentie zelfvoorzienend.*
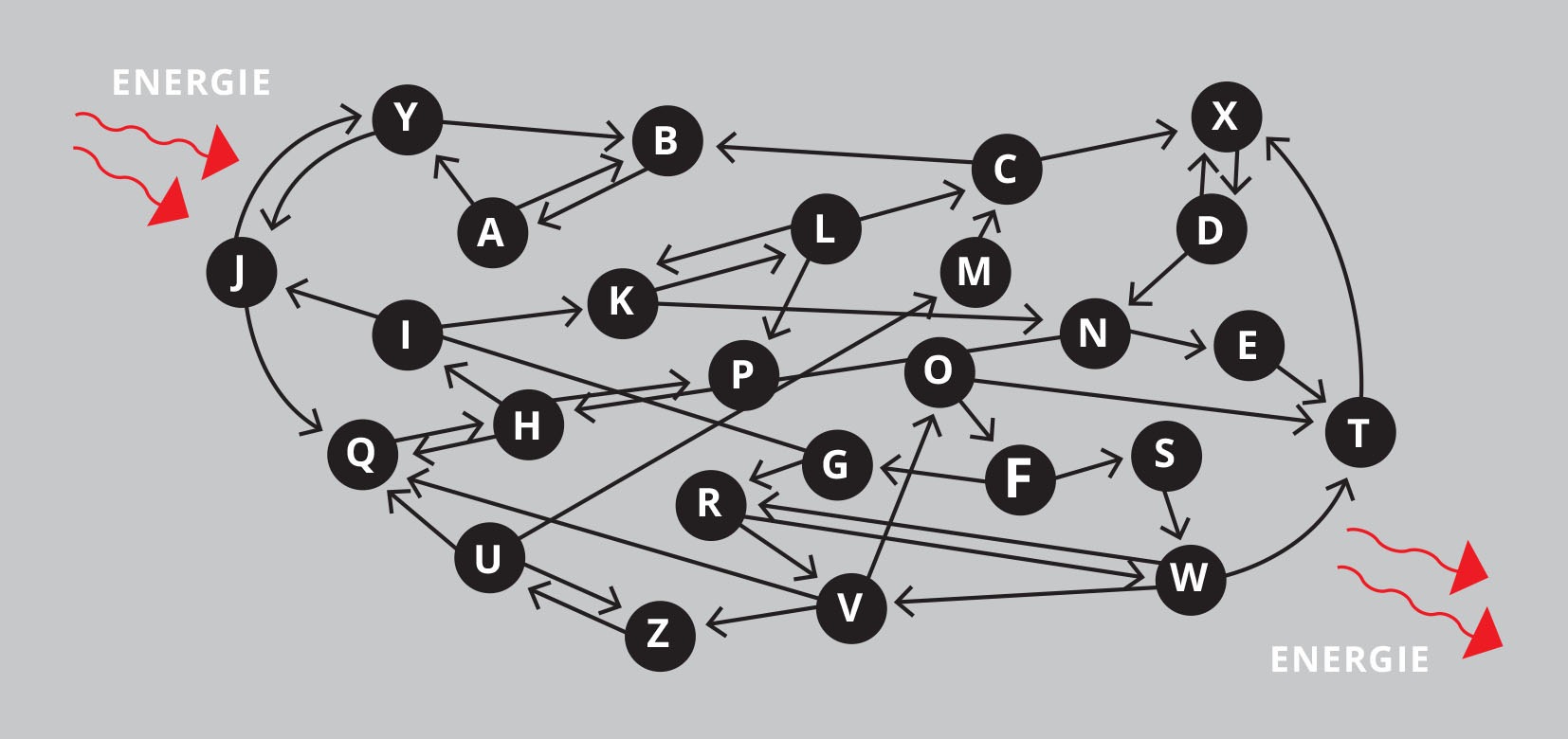
Figuur 2: Een ecosysteem in schema (sterk vereenvoudigde weergave).
Zulke complexe dynamische systemen behelzen ingrediënten van alle ecologische mechanismen die in het veld zijn geïdentificeerd, zoals concurrentie, samenwerking, parasitisme, jacht, symbiose, enzovoort. Al deze processen dragen bij aan de veerkracht van ecosystemen en aan begrenzingen die er ‘in het wild’ worden gehandhaafd aan de populaties van individuele soorten. Bij rijpe complexe ecosystemen heb je geen plagen. (Meer hierover in aflevering 24.)
Gezonde biologische systemen hebben een uitgesproken neiging tot homeostase. Dat wil zeggen dat ze in een bepaald milieu erop uit zijn om vast te houden aan een tamelijk constante set van kenmerken. Dat gebeurt door middel van het principe van negatieve terugkoppeling. Het ziet er schematisch afgebeeld zo uit:
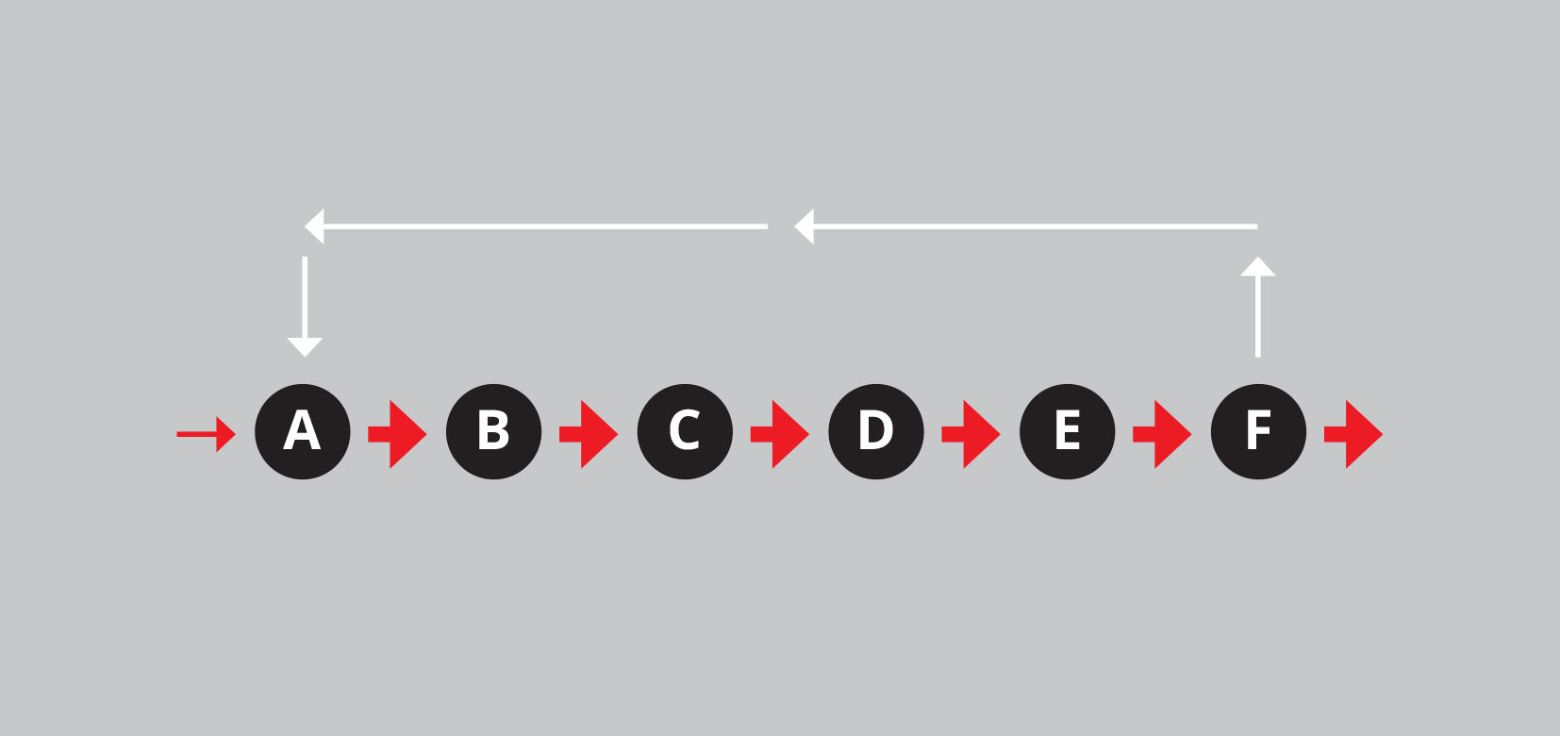
Figuur 3: Negatieve en positieve terugkoppeling in schema.
Onze ademhaling is een voorbeeld van een negatieve terugkoppeling. We weten precies wanneer we opnieuw moeten ademhalen, want de stijging van het kooldioxidegehalte in ons bloed zendt een automatische boodschap naar onze hersenen dat we onze longen aan het werk moeten zetten. Dit is een onbewust proces zoals er in ons lichaam nog ontelbaar meer zijn.
In ecosystemen gaat het al net zo. De terugkoppelingsboodschappen die daar binnen planten en dieren, en tussen planten en dieren, heen en weer schieten, en de antwoorden op die boodschappen, voeden het ecosysteem met terugkoppelingsinformatie.
Wat een vluchtigheid, wat een warboel, wat een zelf-organisatie vind je daar. Sta eens even stil bij welk een dynamische orde een ecosysteem zichzelf oplegt, en welk een dynamische orde onze eigen lichaam ons oplegt zonder dat we dat eigenlijk door hebben.
De natuur biedt bij sociale insecten tal van heldere voorbeelden van perfecte terugkoppelingen. Neem een termietenkolonie. Zo’n kolonie onderhoudt een evenwicht in de omvang van verschillende kasten. Alle termieten worden geboren uit dezelfde soort eieren. Wat er uit die eieren groeit kan fysiek enorm verschillen. Dit hangt af van de functies die uitgevoerd moeten worden. In de babykamer komt de informatie binnen die zich terugkoppelt in chemische stoffen in de larven. Als bijvoorbeeld de volwassen soldaten te weinig van hun specifieke geur afgeven, weet de kolonie dat ze onderbemand is. Er kan geen misverstand bestaan over deze terugkoppeling: er moeten soldaten bijkomen. Daarom komt de babykamer vervolgens met meer soldaten. Zijn er daarna genoeg soldaten, dan rapporteert de geur: ‘nieuwe soldaten zijn niet nodig’. Zo gaat het ook met de andere kasten van de kolonie en blijft de zaak in evenwicht.
Nu over naar expansie, het tweede principe van Jane Jacobs.

Het volume en het gewicht van biomassa op aarde is een verbazingwekkende demonstratie van expansie. Het begon met een barre planeet en nu is er een enorme kluit planten en dieren, inclusief bijna acht miljard mensen. Niet iedereen beseft het, maar het volume van de biomassa bestaat voor driekwart of meer uit micro-organismen. Zoveel massa en diversiteit is natuurlijk onmogelijk als er geen ontwikkeling en co-ontwikkeling zou zijn. De puzzel is: hoe gaat dat? Je zou misschien denken dat iets nieuws dat succesvol is, iets bestaands met een even groot volume verdringt. Maar dat gebeurt niet in de natuur.
Als je de successie van leven op een aanvankelijk kaal veld volgt, dan zie je het volume van de biomassa stap voor stap toenemen. Pionierplanten beginnen de bodem te bedekken, bodemleven begint, er komen struiken, boompjes, jonge boompjes worden groot, dierlijk leven wordt gevarieerder, met wormen en kevers, vogels, kleine zoogdieren, en een heleboel micro-organismen. Hierover gaat het vanaf aflevering 17.
Het lijkt erop dat op een gegeven moment het hele spectrum van levende wezens wel aan boord van deze Ark van Noach is. Toch weet de toename van de biomassa dan nog niet van ophouden. Bomen worden groter, de humuslagen dikker, wormen vetter, schimmelnetwerken robuuster, muizen talrijker en korstmossen zwellen verder op. Wat gebruiken ze voor hun toename? Het rijke milieu? Ze maken het milieu toch juist zelf rijker met hun toename?
Een zogenaamd zichzelf-ondersteunend systeem houdt zich natuurlijk niet echt zélf gaande. Het is geen perpetuum mobile. Er is een inbreng van energie van buiten voor nodig, brandstof. (Dat geldt niet alleen voor zo’n complex levend systeem in de natuur, maar voor elk systeem, ook als het een rivier is, of het oceanisch systeem.) Er moet wat ingestopt worden voor er wat uitkomt, van welke aard dan ook. Maar wat er ook ingestopt wordt, (vrijwel) alles is terug te voeren op zonlicht. In een ecosysteem leven de chloroplasten symbiotisch in de plantencellen. Ze vangen het ‘ruwe’ zonlicht op en vanaf dat beginpunt zijn de injecties van energie die organismen verderop in het web krijgen, omzettingen van die zonne-energie. Over deze fotosynthese gaat het vanaf aflevering 5.
Alle energie die wordt ontvangen, wordt uiteindelijk ook weer afgegeven. Materie is in principe energie die op een specifieke manier verpakt is. Energie/materie kan worden omgezet in diverse vormen, maar niet geschapen of vernietigd worden. Tijdelijke opslag kan wel, bijvoorbeeld in hout, of fossiele brandstoffen, en zelfs in kalksteen. Die opslag kan dus soms lang aanhouden. Maar uiteindelijk komt de energie vrij en straalt het systeem de energie uit, waarmee deze verloren gaat. Tegenover dit verlies móet ook opname (infusie) staan. Dit punt komt terug in aflevering 23 van het tweede artikel, waar het gaat over entropie.
Een ecosysteem kan dus worden opgevat als een soort leidingstelsel waar energie doorheen gaat, met veel of weinig omzettingen van energie/materie in de loop er doorheen. De interessante vraag is dus: wat gebeurt er in het stelsel?
In de woestijn is dat niet veel. Overdag warmt alles op, ’s nachts wordt de hitte weer afgegeven. Leven is er amper. Het rijkst ontwikkeld is het regenwoud-ecosysteem. Hier stroomt de energie bepaald niet snel en simpel. De diverse energetische kronkelwegen weerspiegelen een levensweb waar het krioelt van de relaties tussen van elkaar afhankelijke organismen. Als zonlicht eenmaal in het ‘leidingstelsel’ is opgenomen, wordt het niet slechts omgezet, maar opnieuw omgezet, nog maar eens omgezet, gecombineerd, weer anders gecombineerd, doorgegeven en teruggegeven. Het wordt dus gebruikt en hergebruikt wanneer energie/materie van het ene naar het andere organisme gaat. De energiestroom in dit ingewikkelde stelsel talmt voortdurend en dwaalt steeds af. Bij successie zien we dat stap voor stap toenemen. Deze energie laat in de complexe levenswebben alom tekenen achter dat zij voorbij is gekomen.*
Het principe kan nu als volgt verwoord worden: Expansie steunt op het opvangen en benutten van voorbijgaande energie. Hoe meer verschillende manieren een systeem bezit om energie opnieuw te vangen, te benutten en door te geven voordat deze energie door het systeem wordt afgegeven, des te groter is de optelsom van gevolgen van de ontvangen energie.*
Ook de wetten van de thermodynamica zien we hier aan het werk. Het onvermijdelijke energieverlies drukt zich uit in de noodzaak tot bijtanken.

Systemen moeten ‘zelf-bijtanken’ om aan de gang te blijven. Niet alleen het groeien, ook het lopen van de motor kost brandstof. Dat betekent dat een deel van de energie die van buiten wordt opgenomen, gebruikt wordt om de volgende energie-inname te veroveren, en daarvan wordt weer een deel besteed aan de daaropvolgende energie-inname, enzovoort.
Naast de nóódzaak van bijtanken is een tweede kenmerk van wie zichzelf bijtanken, dat hij/zij/het op een geschikte manier is toegerust voor de brandstof die eraan te pas komt. Een geschikte uitrusting is zo belangrijk dat een falen daarvan voor een organisme net zo fataal is als het verdwijnen van de brandstof. Geschikte uitrusting is het ‘bij’ van bijtanken.
Een koe heeft de juiste uitrusting om gras te eten. Gras is haar brandstof. Voor termieten is de brandstof hout. Een koe kan van hout niet leven. Een geschikte uitrusting omvat de uitrusting om zich van voeding te verzekeren, het te veroveren, plus de uitrusting om het te verteren; vaak komen er symbiotische bacteriën aan te pas. Bij de koe gaat het daarbij om een mond die geschikt is om mee te grazen, een rustige wei of stal, haar vier magen en de bacteriën die daar leven. (Planten werken dan weer samen met schimmels: zie aflevering 30.) Hoe efficiënt een koe ook mag zijn, als zij niet bijtankt, wordt zij een dode koe.*
Vanwege de noodzaak dat uitrusting en brandstof precies op elkaar aansluiten, komt het er bij zelf-bijtank-systemen nauw op aan. Elk systeem heeft zijn eigen ‘integriteit’ als een op zichzelf staande, concrete eenheid. Zichzelf bijtanken doet ieder op zijn eigen manier. Het afval van het ene organisme is een banket voor een ander organisme. Zo is bijtanken een volstrekt natuurlijk proces.
Behalve om ontwikkelen, expanderen en bijtanken gaat het om ‘energetische bestendigheid’. Het betreft de dynamische stabiliteit van alle systemen waar dynamiek in zit: van levende systemen, zoals ecosystemen, en zielloze systemen, zoals rivieren en de atmosfeer. Die dynamische systemen lopen gevaar instabiel te worden. Ze behoeven – het vierde punt van Jane Jacobs – constant zelf-correctie. Ze gaan tenslotte allemaal ten onder, maar het mooie is dat ze het vaak zo lang uithouden. Ze hebben vier middelen om ontwrichting te voorkomen. De eerste is de negatieve terugkoppeling die we al tegenkwamen in aflevering 2. De tweede is positieve terugkoppeling die niet per se ‘negatief’ hoeft uit te pakken.*
Met de komst van de landbouw begon een positieve terugkoppeling die wel fnuikend was, namelijk in de vorm van het verlies aan voedingsstoffen uit de bodem. Dat gebeurde op drie manieren: door de oogst van het land te halen, door uitloging (oplossing in water waarmee ze wegstromen) en door de grond zelf weg te halen. Dat gebeurde natuurlijk meestal allemaal tegelijk. Het constant weghalen van plantaardig materiaal is een positieve terugkoppeling waarmee de boer moet zien te dealen.*
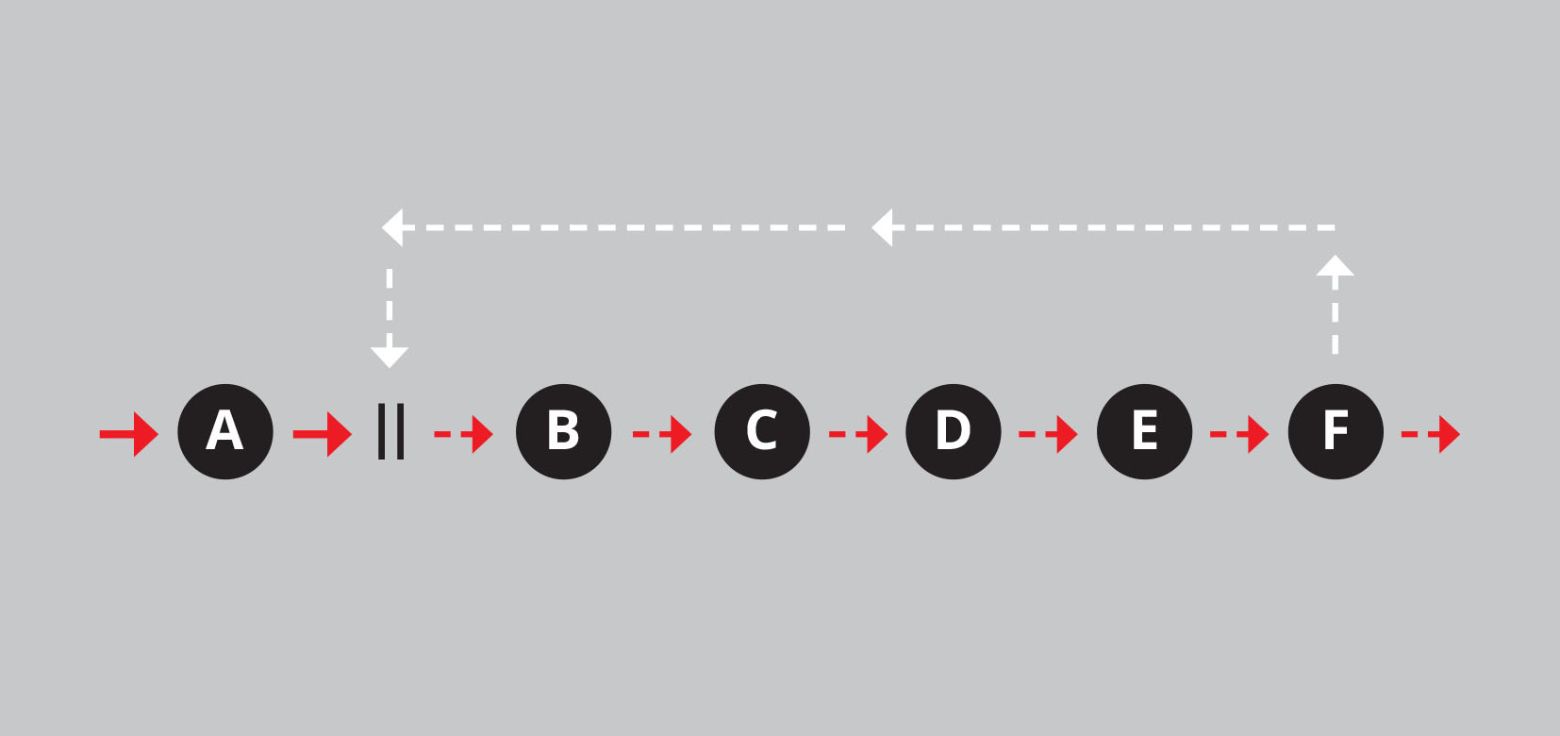
Figuur 4: Negatieve en positieve terugkoppeling in schema.
De twee andere middelen om ontwrichting te voorkomen zijn bifurcatie en noodmaatregelen. Met bifurcaties zijn we al vertrouwd, want bifurcaties zijn ontwikkelingen, maar dan wel onomkeerbare. Bifurcaties worden ook wel discontinuïteiten genoemd. Het zijn nieuwe wegen die een systeem inslaat, waarbij een nieuw terrein betreden wordt. Erna is er geen weg terug. Toen vissen in de loop van de evolutie aan het water ontsnapten door de vorming van longen, was dat misschien om aan roofdieren te ontsnappen die hen op land niet konden volgen. Deze stap gebeurde ergens, op een bepaalde plaats. Want bifurcaties beginnen ‘zomaar’ (anekdotisch), niet als een algemene ommezwaai (statistisch). Dat wil zeggen, succesvolle aanpassingen verspreiden zich van die ene plek omdat degenen met die aanpassingen zich verspreiden.
Bifurcaties hebben complexe gevolgen. Het zijn niet alleen geheel nieuwe praktijken, ze veranderen precies die systemen waar ze ontstaan (of de systemen die deze bifurcaties na-apen). Bifurcaties corrigeren alleen al ze tijdig zijn, in de fase voordat een systeem instort. Later is te laat. De verandering moet als het ware al in de coulissen staan te wachten, bijvoorbeeld in de genen. Dat het noodzakelijk was, heb je achteraf pas door. En: bifurcaties kunnen dan wel heel goed zijn in het corrigeren van instabiliteit, ze brengen zelf ook weer nieuwe vormen van instabiliteit voort.
Zo was het begin van de landbouw een bifurcatie die zich over de wereld verspreidde, die ons nu grote problemen bezorgd – denk aan de problematiek van de stikstof en de waterkwaliteit. Nu deze moderne landbouw zijn einde nadert, staat de regeneratieve landbouw in de coulissen klaar, omdat al zoveel boeren daarmee in de praktijk experimenteren (zie aflevering 22 van het tweede artikel).
Zie over het middel ‘noodmaatregelen’ aflevering 27 van het artikel ‘De natuur van de economie’ van Jane Jacobs in de rubriek Complexiteit.
Vergelijk dit geheel ook met de Wet van Kooijman: aflevering 13 van het artikel ‘De aarde leeft!’ van Peter Westbroek in de rubriek Ecologie.
Nu over naar de plant die als fotosynthetiseerder met het verslaan van de tweede wet van de thermodynamica eigenlijk bleef steken in een bifurcatie die bestendigheid opleverde.

Gaia-onderzoeker Tyler Volk wandelde eens in een botanische tuin in Californië en kwam bij een klein kunstmatig meertje vol eenden en zwanen.* Ik vertaal in aflevering 5-12 met soms een kleine weglating wat hij beschrijft:
Aan de overzijde groeide een bosje met allerlei soorten struiken en bomen. ‘Wat zou de betekenis van al die soorten voor het geheel zijn?’, vroeg Volk zich af. En opeens zag hij één antwoord voor het eerst. Die strook fotosynthetiseerders aan de overkant bracht een visuele boodschap over, de boodschap van een kleur: groen. Al die verschillende soorten voegden zich samen tot een enkele, sprankelende eenheid. Dit groene beest had weliswaar vele onderdelen, maar deze hadden meer weg van de bouwstenen in een muur dan van aparte individuen. Voor de allereerste keer was Volk getroffen door de volle kracht van het biochemisch gilde. En zie je het eenmaal dan zie je het ineens overal, door alle jaargetijden, in extreme omstandigheden, in de vorm van algen, noem maar op. ‘Gaia zit er niet mee dat individuele planten en algen komen en gaan, zolang de aanwezigheid van groen maar eeuwig doorgaat.’
Waarom groen? Elk schoolkind krijgt les over een van de meest welluidende woorden in de wetenschap: ‘chlorofyl’, oftewel bladgroen. Het is een van de belangrijkste moleculen van Gaia. Chlorofyl absorbeert het rode en blauwe einde van het zichtbare spectrum van zonlicht en weerkaatst iets van het midden ervan, in het gebied dat wij groen noemen. Een dicht bladerdek weerkaatst slechts een paar procent van het onderschepte licht, en doordat dit voor het merendeel groen is, overheerst deze kleur voor ons totaal. Maar voor de actieve plant of microbe gaat het niet om wat weerkaatst wordt; het gaat er juist om dat er zoveel van het spectrum daadwerkelijk geabsorbeerd wordt.
Er wordt veel gepraat over wat chlorofyl allemaal kan, maar zelden hoor je over de vorm van het molecuul. Dat ziet er een beetje uit als een platgedrukt kikkervisje. Of lijkt het misschien op een geplette struik met een penwortel? De kop- en staartvorm van chlorofyl is een zaak van functie volgt vorm: de kop ontvangt de energie, de staart levert, net zoals een wortel, het anker. De kop zet de lichtfotonen-energie om in de opgewonden energie van elektronen.* Dat lukt met een geometrie die bijna kristalvormig is: vier pyrrool-ringen in regelmatige vijfhoeken die opgesloten zitten in een grotere porfirine ring. Mooie termen, maar het komt neer op een viervoudige mandala met elk ruwweg dertig koolstofatomen, één waterstofatoom en drie zuurstofatomen, gepeperd met precies vier stikstofatomen, één voor elke pyrrool-ring. In het midden zit een speciaal ingrediënt: één enkel magnesiumatoom. Dit netwerk wordt verder aangevuld met losjes gebonden elektronen die gelaagd in ringen zitten en fotonen kunnen oppikken. Dat gebeurt met verschillende gradaties van doeltreffendheid, afhankelijk van de frequenties. We hebben het hier over figuur 4a.
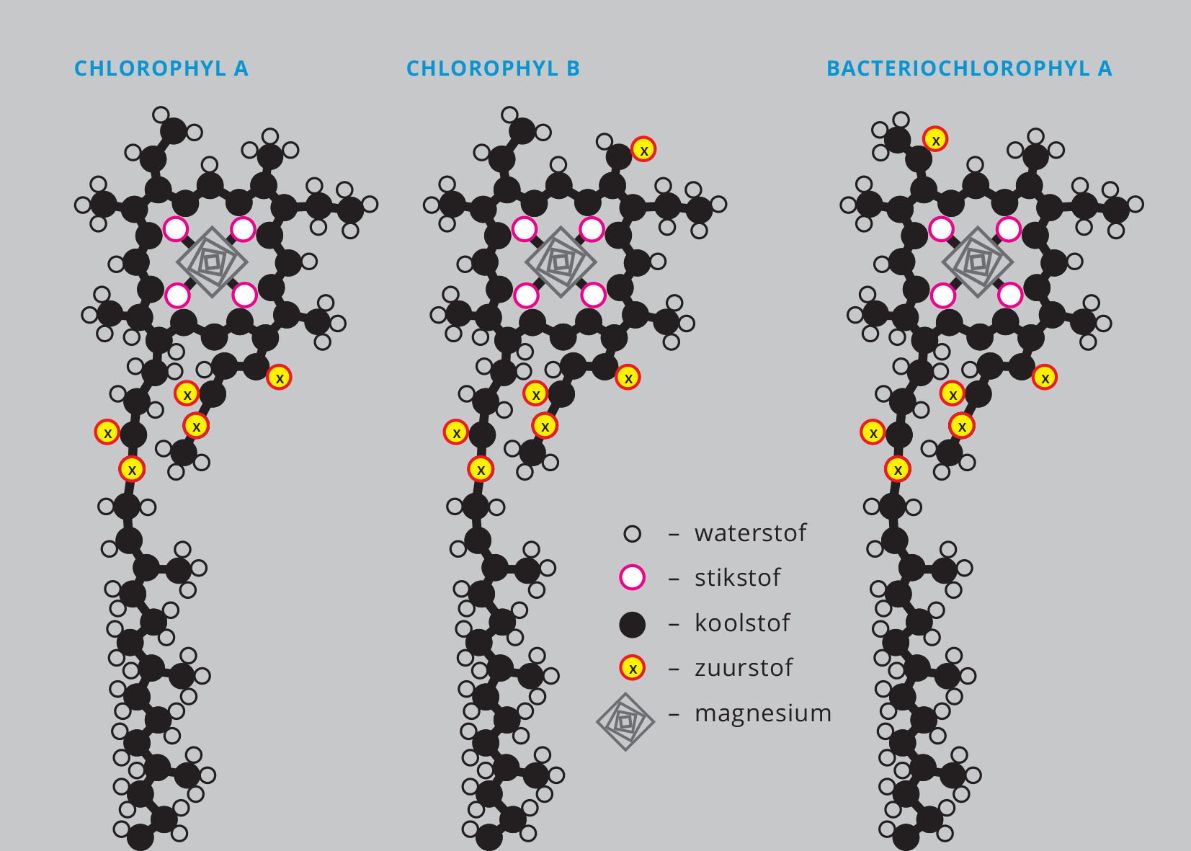
Figuur 5: Drie typen chlorofyl. In de tekst gaat over het type chlorofyl-a. Je hebt dus ook nog een type b en een variant bij fotosynthetiserende bacteriën, die van elkaar verschillen doordat enkele atomen op een andere plaats zitten. En dat is nog niet helemaal het complete rijtje. Het gaat niet om de verschillen maar juist dat ze zoveel overeenkomsten hebben.
De kop van het chlorofyl moet geankerd worden om het als onderdeel van het fotosynthetische systeem naar behoren te laten functioneren. Die taak is toebedeeld aan de staart. Met verhoudingsgewijs meer waterstof dan de kop, bestaat de staart grofweg uit twintig koolstofatomen en twee zuurstofatomen. Deze lipide-achtige (vettige) stof hecht zich vlot aan de lipide-membranen van cellen, een kwestie van soort zoekt soort. De staart kan buigen en draaien aan de moleculen van het cel-membraan, ongeveer zoals een olieachtige, opgerolde handdoek in een rij van net zulke handdoeken. Om te voorkomen dat het chlorofyl opzij gaat hangen zorgen eiwitten die uit het membraan steken en verbonden zitten met het magnesiumatoom middenin de mandala ervoor dat het foton-absorberende gaas in precies de juiste hoek gehouden wordt.
Dat is chlorofyl: 120-en-een-beetje atomen gerangschikt in een binaire structuur – tennisracket-achtige kop en kleverige staart – als buitengewone opslokker van fotonen, in gebruik bij vrijwel alle fotosynthetiseerders – de molecule in de biosfeer waar alles om draait.
En dit is nog maar het begin van dit verhaal.

Hoe is chlorofyl precies in een blad verdeeld? Stel, zegt Tyler Volk, dat je de mensheid vermenigvuldigt met enkele tientallen miljoenen, en dat die mensen chlorofylmoleculen zijn, dan zouden die met gemak een plekje vinden op slechts één vierkante centimeter blad. Dat is dezelfde schaal als de dichtheid van de fotonen die op hetzelfde bladoppervlak botsen. Het stelt elke chlorofylmolecuul in staat om uit de stortbui van helder zonlicht per seconde enkele fotonen te absorberen. Elke absorberende molecule-kop licht op in een opgewonden toestand met zo’n beetje het tempo van de hartslag van iemand bij een pittige aerobics-oefening.
Die talrijke absorbeerders zitten niet zomaar door elkaar, maar op een paar uitzonderingen na weten we niet precies hoe ze gerangschikt zitten. Wel weten we dat er meer chlorofylmoleculen zijn dan plekken in de basis om de fotosynthese uit te voeren. Hun werk moet gebundeld worden. Chlorofylmoleculen zijn slechts de eerste stap in een ingewikkeld proces van het algehele fotosynthese-systeem in een cel. Het is in elk geval zo dat een paar honderd chlorofylmoleculen samen een veelzijdige ‘antenne’ vormen die alle opgevangen energie naar één enkele plek overbrengt, het reactiecentrum.
Elk chlorofylmolecuul dat energie opvangt, vormt een soort schakel, net als in een brigade die emmers bluswater doorgeeft. Of zie het als een stelsel regenpijpen waarbij het water van elke pijp in een centraal gat bij het verzamelde water uit de andere pijpen samenkomt. Alleen wordt hier geen water doorgegeven maar resonantie. Steeds brengt een vibrerend chlorofylmolecuul zijn opwinding over naar een buurman en wordt daar zelf kalmer van. Deze trechter van geactiveerde elektronbesmetting is wel vergeleken met de energie-overdracht tussen aangrenzende stemvorken.
Hoe de resonantie-overdracht weet dat hij altijd in de richting van het reactiecentrum moet bewegen, en niet ervan af, is tegelijk fascinerend en niet helemaal duidelijk. Hier wordt de stroom niet door de zwaartekracht aangedreven, zoals bij de regenpijpen, maar door entropie – die spontane overgang naar een lagere-energie-toestand (zoals de geleidende stroom hitte die een versgebakken brood afgeeft). Op die manier kan de energie van het ene chlorofylmolecuul op de buurman overspringen als die buurman minder opgewonden is, wat wil zeggen dat zijn natuurlijke vibratietempo lager is. Ongelijkheden in het vibratietempo (de frequentie) verlenen de stroom richting. Bij de overdracht gaat wel wat energie verloren; dat is de prijs die voor de gerichtheid betaald wordt. Bij de paarse zwavelbacteriën, die in dit opzicht het best bestudeerd zijn, zijn de chlorofylmoleculen ingesteld op drie verschillende frequenties, waarbij de netwerken met de hogere frequenties verbonden zijn met de netwerken met de lagere frequenties. De aangelegen eiwitmoleculen, die verbonden zijn met de centrale magnesiumatomen in de chlorofylmoleculen, spelen een essentiële rol bij het afstemmen van de frequenties; kennelijk kunnen ze de spanning (en daarmee de frequentie) van hun zon-vangende mandala-mazen beheersen.
Er is nog een tweede klasse pigmenten die meehelpt, de carotenoïden. De bekendste is bètacaroteen. Die zit in worteltjes, pompoenen en papaja’s. Maar bètacaroteen zit ook in de meeste groene bladeren; alleen wordt de aanwezigheid ervan daar gemaskeerd door het chlorofyl. Uit hun andere kleur kun je al opmaken dat carotenoïden licht heel anders absorberen dan chlorofyl. Speciaal hun blauwe absorptie is wat naar het groen opgeschoven. Zonder carotenoïden zouden minder efficiënte bladeren de ‘blues’ zingen. Daarbij missen carotenoïden dan weer het stuk van de rode absorptie dat chlorofyl heeft. Zij reflecteren daarom de ‘warme’ frequenties van het licht. Afhankelijk van het type gloeien ze in de herfstbladeren als rood, oranje, bruin of geel, want chlorofyl is het eerste pigment dat in een stervend blad vervaagt. In de meeste chlorofyl bevattende fotosynthetiseerders zitten carotenoïden die de fotosynthetische machine de kracht geven om de fotonen op te pikken die chlorofyl anders zou missen. Ze doen dus mee aan de emmerbrigade.*
Zo vinden we stap voor stap uit hoe de natuur de tweede wet van de thermodynamica een loer draait.
De opgevangen energie komt uiteindelijk terecht in de reactiecentra. Dat zijn strak geïntegreerde eenheden van verschillende moleculen waarmee de binnenkanten van de membranen, die tot de cel behoren, bezaaid zijn. In zo’n reactiecentrum maakt chlorofyl opnieuw zijn opwachting. Chlorofyl bezet het midden van het reactiecentrum, vastgehouden door een steigerwerk van eiwitten en beroerd door een doolhof van gevoelige moleculen, die stuk voor stuk opgewekt kunnen worden om elektronen op te nemen en weer los te laten. Dit chlorofyl in het midden (dat bijna altijd een uniek afgestemd, gebonden paar vormt), kun je zien als het gat in de trechter waardoor de energie uiteindelijk naar een andere toestand zoeft. Wanneer de emmerbrigade culmineert in de resonantie-overdracht op het centrale chlorofyl, doet die energie een elektron overspringen naar een naburig acceptormolecuul. In het volgende 200 biljoenste deel van een seconde zigzagt het elektron door een doolhof van acceptoren. Een reactorcentrum dat met zulke snelheden werkt, kan met gemak de energiestroom aan die een reeks van een paar honderd chlorofylmoleculen kan verzamelen. Ergens in deze vlaag van activiteiten, met moleculen die in opgewonden toestand worden gebracht door rijen van overspringende elektronen, worden watermoleculen in waterstofionen, elektronen en zuurstof gehakt. Het eindresultaat van de reactiecentrumfabriek is dat de negatief geladen elektronen naar de ene kant van het membraan worden geschoven en de positief geleden waterstofionen naar de andere kant. (Elektronen die over zijn worden naar het chlorofyl teruggebracht om degenen die verloren gingen te vervangen.) De vangst van energie, die begon als fotonen en hun beteugeling in een vorm die voor de cel werkzaam en bruikbaar is, wordt met deze scheiding van lading afgerond. Houd in gedachten dat het ultieme doel van de fotosynthese het benutten van lichtenergie is om de kooldioxide en het uit water afkomstige waterstof aan elkaar te lassen (zoals in de formule 6H₂O + 6CO₂ C6H12O6 + 6CO₂ waarnaar de titel van deze aflevering verwijst) en het resultaat dan vast te rijgen in ketens van complexe koolwaterstoffen en andere moleculen. Maar zover zijn we nu nog niet.
Carotenoïden spelen ook een cruciale rol in het watersplitsende reactorcentrum, meerdere rollen zelfs. Sommige helpen de minifabriek te beschermen tegen schade die hij zichzelf aandoet. Als de pijplijn met elektronen voor het reactiecentrum verstopt raakt – en dat gebeurt soms – dan heeft het geproduceerde zuurstof soms een elektron in superopgewonden staat. Als een dolle hond kan het een ravage aanrichten. Naburige beschermende carotenoïden absorberen dan de energie van zo’n opgewonden zuurstofelektron en verspreiden de energie als onschadelijke warmte. Als alles naar behoren gaat – en dat is meestal het geval – stroomt moleculaire zuurstof als gas het organisme uit. Bij een nietige blauwalg passeert de zuurstof het buitenste membraan naar de oceaan om ten slotte naar de lucht ontsnappen. Bij een cel binnen in een dennennaald komt de zuurstof in de lucht tussen de cellen, waarna het door een huidmondje de atmosfeer in zweeft. Zo is het watersplitsende reactiecentrum de verbinding tussen de moleculaire energetica van chlorofyl en de atmosfeer.
In alle fotosynthetiserende organismen die zuurstof genereren, van de microscopische blauwalg tot de torenhoge dennenboom, reizen de elektronen van het gesplitste water door naar een tweede reactiecentrum, een heel ander type. Rondom deze tweede assemblage van eiwitten en speciale acceptor/donor-moleculen zit een eigen reeks chlorofyl, die meer fotonen vangt en de verstrikte energie in een anders afgestemd chlorofylpaar het ‘centrum van het centrum’ in trechtert. In dit tweede type reactiecentrum wordt de energie van de arriverende elektronen en de bijkomende energie uit de trechter uiteindelijk in een echte, solide chemische verbinding gerangeerd: nicotinamide-adenine-dinucleotide-fosfaat (NADPH, in de Engelse afkorting met de PH van phosphate). We kunnen dit reactiecentrum daarom betitelen als het energieverpakkingsreactiecentrum. In een ander type moleculaire fabriek vlakbij wordt adenosine-trifosfaat gesynthetiseerd (afgekort als ATP). Dit centrum ontvangt de daarvoor benodigde energie uit het kanaliseren van de waterstofionen die van het eerste watersplitsingsreactiecentrum afkomen. Samen zullen deze twee energie-opslag-moleculen (ATP en NADPH) gebruikt worden om met biosynthese suiker te vormen, dat weer cruciaal is voor de energie voor alles wat er in het fotosynthetiserende organisme nog opgebouwd wordt.
Energie wordt hier omgezet in materie, een reactie die soms dus weer wordt omgekeerd.

Volk maakt vervolgens onderscheid tussen enkele varianten chlorofyl, maar concludeert: Alles bij elkaar ontkom je er niet aan om onder de indruk te raken van het starre conservatisme van de fotosynthetiserende systemen. (Beschouw conservatisme hier als consistentie door heel de verscheidenheid van het leven.) Neem het feit dat alle zuurstofvoortbrengende fotosynthetiseerders die tot dusverre bestudeerd zijn, de combinatie van de twee centra vertonen, die van de watersplitsing en die van de energieverpakking. Neem daarbij dat de carotenoïde helpers vrijwel universeel voorkomen. Neem de alomtegenwoordigheid van chlorofyl, niet slechts in de grote verscheidenheid van zuurstofgeneratoren van blauwalgen tot dennenbomen, maar ook in alle anaerobe bacteriële fotosynthetiseerders (die we hier verder onbesproken lieten). Het is waar dat er verschillende typen chlorofyl nodig zijn om al deze rangen te vullen, maar de kleine verschillen tussen die typen getuigen juist van hun nauwe moleculaire en evolutionaire verwantschap.
Dan is er nog een aantal punten dat het ontzagwekkende toont van de centrale plaats die de rol van chlorofyl-a zelf inneemt. Om te beginnen hebben alle zuurstofgeneratoren chlorofyl-a. Ten tweede wordt in de biochemie van de cel chlorofyl-a het eerst gesynthetiseerd en worden de andere typen (zelfs de bacteriële) ervan afgeleid. Chlorofyl-a ging daarom vermoedelijk niet slechts de andere typen voor in de gang van de cellulaire biochemie, maar vormt ook in de evolutie de voorloper. Ja, want ondanks het aantrekkelijke idee dat in het vroege begin van het leven, toen er nog weinig zuurstofgas in de atmosfeer zat, de anaerobische fotosynthetiseerders de aerobische vooraf zouden zijn gegaan, bekijken veel wetenschappers de blauwalgen, met hun aparte chlorofyl-a, eerder als evolutionaire voorlopers. Misschien zijn zij zelfs al verschenen bij het prille begin van het leven. De centrale rol van chlorofyl-a blijkt, ten derde, ook uit het feit dat het het uiteindelijke doel van de verzamelende trechter is, met het duo op de troon in het centrum van beide typen reactiecentra van de zuurstof voortbrengende fotosynthetiseerders. We zien dat het conservatisme van chlorofyl het spreekwoord volgt: ‘ga niet kloten aan iets wat het goed doet’.
De wereldwijde aanwezigheid van chlorofyl impliceert iets van wereldwijde genen. Het is echter niet gepast om van een ‘groen gen’ te spreken, want chlorofyl is geen eiwit. Slechts eiwitten die gemaakt zijn uit aminozuren kunnen beschouwd worden als direct gecodeerd door de genen in het DNA. Chlorofyl kun je eerder bekijken als het bouwresultaat van een complexe wisselwerking tussen eiwitten met de aard van enzymen. (Eiwitten die andere moleculen opknippen en vastklikken eindigen met hun naam gewoonlijk op -ase). Zo is het inbrengen van een magnesium-atoom in elke mandalacirkel een voorbeeld van een essentiële stap in de cellulaire synthese van chlorofyl. Dit precieze werk wordt uitgevoerd door het enzym magnesium-chelase. Je kunt gerust spreken van een gen voor magnesium-chelase. Zo’n gen is er dus wereldwijd. Het mag dan over de levensterreinen wat variëren, zijn universele rol om magnesium in te brengen houdt in dat alle verschillende structuren van het enzym nauw verwant zijn. Chlorofyl wordt opgebouwd door een systeem van in wisselwerking zijnde enzymen, en daarom zit er achter dit groene pigment niet één enkel gen, maar een systeem van wereldwijde genen. Net zo moeten we wereldwijde families van genen voor carotenoïden onderkennen en voor een paar andere moleculen in de reactiecentra. Dat deze genen universeel zijn voor de enzymen die zij coderen, levert een universeel apparaat op in Gaia’s stofwisseling, een fotonoogster met een planetaire strekking, onderhouden door het biochemische gilde van fotosynthetiseerders.
Betekent dit nu dat de bifurcatie naar chlorofyl geen verdere ontwikkeling meer heeft opgeleverd, of is verdere ontwikkeling gesneuveld als evolutionair minder gunstig?

Tot nu toe hebben we gekeken hoe in de fotosynthese steeds wat water wordt opgesplitst om wat energie-opslag-moleculen te maken – we keken dus naar het deel ‘foto’ uit het woord fotosynthese. Laten we nu kijken hoe in de ‘synthese’ met toevoeging van kooldioxide de biomassa gebouwd wordt die eikenbomen zo fier overeind doet staan.
Bij de synthese wordt de koolstof uit kooldioxide ingebracht om organische moleculen te maken. Zonder deze cruciale eerste stap zou het opnemen van stikstof, fosfor, ijzer, magnesium, of elk van de voedingselementen die er nog meer zijn, net zo zinloos zijn als het hebben van kleren zonder een lichaam. De inpassing van koolstof wordt bereikt door de zogenaamde ‘donkere reacties’, die niet zo heten omdat ze in het donker plaats vinden (al kan dat wel), maar omdat ze niet direct aangedreven worden door fotonenergie. In plaats daarvan zijn de energie-opslag-moleculen NADPH en ATP hun krachtbronnen; we bespraken ze in aflevering 7.
De donkere reacties beginnen bij een ander, alomtegenwoordig molecuul met de bijna onuitsprekelijke naam ribulose-1,5-bifosfaat-carboxylase-oxygenase. Die naam wordt afgekort tot Rubisco. Het is een kolossaal eiwit, een macromolecuul, met onderdelen die zelf ook weer grote eiwitten zijn. Dit enzym weegt 500.000 keer zoveel als een waterstofatoom en 700 keer zoveel als chlorofyl. Erbinnen zijn zo’n 50.000 atomen – voornamelijk waterstof, koolstof, zuurstof en stikstof, dat wil zeggen de normale bouwstenen van een eiwit – met elkaar verbonden door middel van een holarchie van schalen.* Ze vormen een grote bal met naar buiten stekende bulten en ingevouwen dalen qua vorm en lading.
Rubisco is niet alleen groot, maar komt ook veel voor. Het krijgt vaak het predicaat van het meest verspreide individuele eiwit in de biosfeer. Als je op een vers blaadje sla kauwt, zou de helft van het eiwit dat je binnen krijgt Rubisco kunnen zijn.
Zoals de naam al aangeeft is Rubisco een carboxylase. Dat wil zeggen, het bevordert carboxylatie, oftewel het verbinden van kooldioxide met iets anders. Dat ‘iets anders’ is ribulose-1,5-bifosfaat (afgekort als RuBP). Als enzym heeft Rubisco de eigenschap om hun potentiële paringsplaats zo in te richten dat een snelle en effectieve versmelting tot stand komt. Rubisco is als een luxe uitgaansoord dat trouwlustige singles van over de hele wereld samenbrengt; het levert de omgeving voor een natuurlijk moleculair ja-woord. Stel je die enorme Rubisco voor die zowel het priegelige kooldioxidemolecuul als het iets grotere RuBP (26 atomen) tussen verscheidene van haar bulten omarmt, zodat de kleinere moleculen in de vouwen in elkaar klikken. Het is een chemische reactie die klaar staat om plaats te vinden, als de twee ‘ja-klikkers’ elkaar maar weten te vinden en aan te raken. Rubisco vervult hier de essentiële rol van huwelijksmakelaar. Maar houdt het huwelijk stand?
Nee, er volgt snel een scheiding. Het RuBP-CO₂-systeem is wankel en scheidt zich meteen weer in twee moleculen fosfoglyceraat, (een eerlijke scheiding in gemeenschap van goederen). Deze moleculen zijn stabiel. Dus gebeurt er niets totdat andere enzymen zich aandienen. Daarbij kunnen de fosfoglyceraten in het web van de zogeheten Calvin-cyclus van chemische omzettingen terechtkomen. De energie-opslag-moleculen die in de reactiecentra van de fotosynthese zijn gemaakt, komen er in deze cyclus ook aan te pas; ze zijn nodig om onderweg een paar stappen aan te drijven. Ongeveer halverwege de cyclus wordt er een spiksplinternieuw suikermolecuul afgepeld. Het suiker volgt dan andere cellulaire paden die het kunnen ombouwen naar zetmeel en dan naar cellulose of een hele groep andere verbindingen. Sommige suikers worden met ademhaling verbrand om meer energie-opslag-moleculen te vormen voor de enorme verscheidenheid aan synthese-reacties die in organismen nodig zijn, zelfs voor het maken voor meer Rubisco en chlorofyl.
Met de werking van carboxylase hebben we de gunstige de helft van het werk van Rubisco gehad. Nu de ongunstige helft, de werking van oxygenase.

Behalve een carboxylase (dat het kooldioxide koppelt) is Rubisco ook een oxygenase, dat het vermogen heeft om de versmelting van zuurstof met RuBP te katalyseren. En dat klinkt vreemd, want je verbinden met zuurstof opent gewoonlijk de deur naar verwoesting. En het doet af aan de score van netto-koolstof-winst. Waarom zou de natuur een enzym creëren dat – als een Hindoe-godheid – eerst schept en dan een deel van de schepping vernietigt?
Het lijkt er op dat de oxygenase-activiteit een teken is van de diepe evolutionaire wortels van Rubisco. Fotosynthese kwam vermoedelijk heel vroeg in de geschiedenis van het leven op. Dat was in een tijd toen de atmosfeer nog rijk aan kooldioxide was en zeer arm aan zuurstof. Welk van de twee enzymatische sleepboten – carboxylase of oxygenase – overheerst, wordt bepaald door de uitkomst van een soort chemische competitie, die de ene of de andere kant op wordt getrokken door de concentraties van respectievelijk kooldioxide en zuurstof binnenin de cel, die dan weer nauw verbonden zijn met de concentraties in de omringende en binnendringende atmosfeer. De invloed van de huidige (zuurstofrijke) atmosfeer op de meeste plantensoorten komt erop neer dat oxygenase een opmerkelijke 30 procent van de winst van carboxylase zomaar teniet doet.
In proeven met tarwe in ruimtes met gecontroleerde concentraties is vastgesteld dat meer kooldioxide de groei bevordert. Dat komt doordat de hogere kooldioxideconcentratie de carboxylase-activiteit opkrikt in verhouding tot de oxygenase-activiteit. Het is interessant dat dezelfde winst bereikt kan worden door het zuurstofniveau in die kamers te verlagen. Dit vermindert de oxygenase-activiteit ten opzichte van die van de carboxylase. De manier waarop doet er niet toe, het resultaat is in beide gevallen een betere groei van tarwe. Als het leven begon in omstandigheden met veel kooldioxide en nauwelijks zuurstof, dan zou de oxygenase-activiteit van het zojuist geëvolueerde Rubisco, al was het in potentie aanwezig, toen praktisch op nul zijn uitgekomen. Er zou geen selectiedruk hebben bestaan om een enzym te creëren waar de oxygenase-activiteit van af was gehaald. En toen het zuurstofgehalte begon te stijgen, was Rubisco zijn rol om het koolstof op te nemen kennelijk te zeer toegedaan om evolutionair op een fundamentele manier op zijn schreden terug te keren.
Er is ook nog een andere theorie: de oxygenase-activiteit van Rubisco zou de fotosynthese dienen met dezelfde verbetenheid als een coyote die, gevangen in een klem, liever zijn poot afbijt. Als de voorziening in kooldioxide zou ontbreken en de keten van deelnemers in de Calvin-cyclus het gevaar loopt om in te storten, dan kan Rubisco’s vermogen om RuBP zuurstof te geven (te oxygeneren) – wat zowel tot kooldioxide als fosforglyceraten leidt – tenminste tijdelijk voor een alternatieve bevoorrading van de massa in de Calvin-cyclus-fabriek zorgen, zodat die aan de gang blijft. Deze zelfverbranding van gefabriceerde moleculen in het eigen ademhalingsvuur van de plant schijnt te helpen om de meer vitale delen van het geheel in stand te houden.*
Of het nu een ongewenst restant van de evolutie is of een cruciale veiligheidsklep (misschien is het een beetje van beide), in de huidige atmosfeer leidt de oxygenase-activiteit van Rubisco tot een fotosynthese die de hoogst mogelijke graad duidelijk niet haalt. Maar sommige levensvormen hebben manieren ontwikkeld om de ‘atmosfeer’ binnenin henzelf te optimaliseren – met andere woorden hun interne omgeving rondom de werking van hun Calvin-cyclus. Veel aquatische algen kunnen bijvoorbeeld met miniatuur kooldioxidepompjes in hun buitenste membranen opgelost kooldioxide in zichzelf concentreren. Blauwalgen hebben ook van dat soort moleculaire pompjes. Het gemeten kooldioxide binnenin blauwalgen kan wel tot het duizendvoudige worden opgeschroefd. Met zo’n intensiteit valt de oxygenase-activiteit van Rubisco in het niet.
In het hier beschreven reguliere pad van de fotosynthese draagt het fosfoglyceraat na de splijting van de onstabiele RuBP-kooldioxide-eenheid drie koolstofatomen. Planten die dit pad volgen duidt men aan met de code C3. Bij tenminste 18 verschillende families van landplanten is een fascinerende methode gevonden om intern de kooldioxideconcentratie op te voeren. Dit is de zogeheten fotosynthetische-weg met de code C4. Zo heb je dus C3- en C4-planten.* Het lijkt een evolutionaire aanpassing die waarschijnlijk zo’n tien miljoen jaar geleden plaatsvond (maar dan wel parallel in heel wat soorten) in een tijd dat er veel meer kooldioxide in de atmosfeer zat dan nu. De methode heeft voor de plant voor- en nadelen. Tarwe is een C3-plant, maïs, sorghum en suikerriet zijn C4-planten.
Laten we nu eerst bekijken hoeveel van het zonlicht de plant weet te benutten, voor we in aflevering 13 en 14 bekijken hoe de mens tegen dit suboptimale Rubisco-proces aankijkt.

Het verhaal van de zogenaamde energiecascade begint bij de hoeveelheid zonlicht die op de aarde valt, en eindigt met een klein deel dat de fotosynthese bereikt. Het zonlicht dat de aarde bereikt kun je uitdrukken als energie per oppervlakte-eenheid per jaar: het is zo’n 340 watt per vierkante meter (de donkere helft van de planeet en de verschillen tussen de tropen en de polen meegerekend). Dat is de situatie aan de buitenkant van de atmosfeer. Daarvan wordt direct al 30 procent van gereflecteerd, zodat 240 watt (verder steeds per vierkante meter) binnendringt.* Die energie bereikt zeker niet in zijn geheel het aardoppervlak. Wolken nemen 15 watt op, stofdeeltjes in de wind en verschillende gassen (zoals ozon en waterdamp) vangen nog eens 55 watt weg. Dus 170 watt bereikt tenslotte de aardbodem en het oppervlak van de oceanen.
De helft van de oorspronkelijke 340 watt is dus theoretisch over voor de fotosynthese. Laten we eerst naar het land kijken en aannemen dat er dichte begroeiing is, zoals in de vorm van het bladerdek van een naaldbos of regenwoud, of zelfs een weelderig grasland. Experimenten laten zien dat de opname dan kan oplopen tot 98 procent van de typen fotonen die de fotosynthese aan de gang houden. Daar gaat dus amper wat verloren.
Nu moeten we kijken naar de kwaliteit van het neerkomende licht. Niet alle fotonen zijn levendig genoeg om de chlorofylmoleculen te laten dansen. Zonlicht is verdeeld over een spectrum dat loopt van hoge energie (met hoge frequenties en korte golflengtes) naar lage energie (met lage frequenties en lange golflengtes) – in kleur gezien van ultraviolet en blauw langs groen naar rood en infrarood. Planten kunnen alleen frequenties boven een bepaald minimum absorberen (dus met golflengtes onder een zeker maximum). De cruciale frequentie ligt rond de 430 biljoen cycli per seconde; dat komt overeen met een golflengte van 700 nanometer (700 miljardste van een meter). Alle licht met een golflengte die langer is dan 700 nanometer is onbruikbaar, want te zwak om chlorofylmoleculen in opwinding te brengen. Daarmee valt meteen al 57 procent af.
Een tweede vorm van verlies heeft te maken met de onvolmaakte kwaliteit van de fotonen die de chlorofyl-antenne door de trechter naar de reactiecentra stuurt. Dat proces kost sowieso al wat energie. In de laatste stap zijn de uiteindelijke chlorofylmoleculen in de reactiecentra afgestemd op die 700 nanometer om te absorberen (daar komt het getal in de vorige alinea vandaan). Wat de oorspronkelijke energie-inhoud van de foton oorspronkelijk ook was, hier telt alleen dat deel van de energie mee dat overeenstemt met de frequentie waarbij de centrale chlorofylmoleculen de uiteindelijke overdracht maken. Het valt te berekenen dat dit 80 procent is.
We begonnen met 170 watt per vierkante meter en een ideaal bladerdek; daarvan is 43 procent fotosynthetisch actief en 80 procent daarvan komt ook echt door. Zo houden we nog 60 watt per vierkante meter over. En de energiecascade gaat nog verder.
De volgende stap draait om de ‘quantum-opbrengst’. Hoeveel fotonen (quanta) zijn er nodig om een enkel koolstofatoom in een suikermolecuul te plaatsen, zoals dat op het weefgetouw van de Calvin-cyclus geweven wordt? Theoretisch valt het ‘potentieel haalbare’ op precies 8 stuks te berekenen, maar deskundigen denken dat er in de praktijk misschien wel minimaal 12 fotonen voor nodig zijn. Uit de verhouding van de vastgelegde energie van een koolstofatoom in een gefotosynthetiseerde suikermolecuul en de energie van 12 fotonen valt te berekenen dat de maximale efficiëntie voor de quantum-opbrengst ongeveer 30 procent is.
En dan is er nog de prijs van de oxygenase-activiteit uit de vorige aflevering, die 30 procent van de winst van carboxylase teniet doet. Rekening houdend met het onderscheid in C3- en C4-planten uit het slot van die aflevering kan dat verlies op 20 procent gesteld worden.
Van de 60 watt overleeft eerst slechts 30 procent en daarvan blijft dan weer 80 procent over. Het eindresultaat lijkt dus uit te komen op 14 watt per vierkante meter.
Dit is de hoeveelheid waarop de door de fotosynthese in de primaire suikers vervatte energie theoretisch kan uitkomen. Maar dan heb je het bouwproces zelf nog. En de brute praktijk (tegenover de theorie).

De suikers uit de fotosynthese komen de netwerken van bladeren en dergelijke binnen om te dienen als bouwmateriaal voor cellulose, hemicellulose (voor de celwand), lignine (houtstof) en voor de duizenden typen eiwitten. Voor het knippen en plakken en het snoeien en lassen bij al die moleculaire reacties zelf is ook best veel energie nodig. Daartoe wordt suiker verbrand met zuurstof en uitgeademd als kooldioxide. Om hoeveel gaat het? Dat hangt erg af van het type plant en zijn leeftijd, en ook van de milieu-omstandigheden, zoals de aard van de bodem, de temperatuur en het licht. Maar een goed wereldwijd gemiddelde is: ongeveer de helft. De helft van de primaire suikers moet worden verbrand om de synthese van al die verschillende moleculen en structuren die wij een plant noemen, aan te jagen. In deze laatste stap in de energiecascade moeten we de 14 watt per vierkante meter dus halveren tot 7 watt. Dat is 2 procent van de 340 watt die bovenop de atmosfeer terecht komt. Het is de maximale mate van de belichaming van planten die op deze wereld haalbaar is. Dat is, zeg maar, de theorie.
Hoe is het in de praktijk? Dan moet je de werkelijke productie van biomassa op aarde vergelijken met de theoretisch haalbare. Die productie is zo’n 60 miljard ton aan gefotosynthetiseerde koolstof per jaar, oftewel 132 miljard ton als de zuurstof, waterstof, stikstof en alle andere noodzakelijke elementen worden meegeteld. Dit gewicht kunnen we dan weer omrekenen naar het equivalent aan energie. Dat is 20 miljard joule per ton verdeeld over een gebied van 117 miljoen vierkante kilometer (van het land zonder de woestijnen en bevroren gebieden). Dat draait uit op 0,7 watt per vierkante meter. De werkelijke hoeveelheid blijkt dus slechts een-tiende van de potentieel haalbare 7 watt (van het mooie bladerdek).
Vanwaar dat grote verschil?
Dat komt door de omstandigheden. De natste ecosystemen zijn bijvoorbeeld tweemaal zo productief als ecosystemen die de gemiddelde neerslag op aarde van zo’n 75 centimeter per jaar ontvangen – ongeveer de Nederlandse situatie (van voor de klimaatverandering). De potentiële productiviteit kun je dus vanwege watertekort halveren.
De algehele stilstand vanwege de winter is een andere beperkende factor. De helft van al het land ligt in een brede tropische gordel waar de fotosynthese het hele jaar door aan de gang blijft. Maar op het land boven de 30 gradengrens, dat voornamelijk op het noordelijk halfrond ligt, wordt de fotosynthese steeds minder. New York, dat op 40 graden noorderbreedte ligt, krijgt in het groeiseizoen vanaf mei tot en met september bijvoorbeeld 60 procent van de totale zonnestraling van het hele jaar binnen.* En nog verder naar het noorden is het van juni tot augustus de helft. Deze beperking in de tijd komt voor de activiteit van de fotosynthese gemiddeld uit op 80 procent.
Dan zijn er nog diverse andere factoren die de plantproductie beperken – het levert een filter van 85 procent. En er zijn de voedingsstoffen. Die komen bij Volk uit op 30 procent. Enerzijds verklaart dat het verschil dat we vonden tussen 7 watt en 0,7 watt vrij goed. (Namelijk 7 x 0,5 = 3,5 x 0,8 = 2,8 x 0,85 = 2,4 x 0,3 = 0,7 watt) Tegelijk laat het zien dat ideale voedingsstofomstandigheden de productiviteit verdrievoudigen.
Ten slotte nog een paar woorden over de omstandigheden op zee. Het gaat dan om groen plankton. Planktoncellen dartelen nogal door het water en zijn nooit zo dicht gezaaid als de plantencellen in een bos of een weide. De fotosynthesecapaciteit is in zee dus duidelijk minder. Het mankeert in zee ook vaak aan voedingsstoffen. Daar staat tegenover dat er nooit gebrek aan water heerst en dat plankton dat bijzondere vermogen heeft om kooldioxide in zijn lichaam te concentreren waardoor het verlies van de oxygenase-activiteit van Rubisco omzeild wordt. Zo is er berekend dat de oceanen zo’n twee derde van de biomassa van het land produceren, zo’n 40 miljard ton koolstof, of 88 miljard ton aan totale biomassa (ook al is hun oppervlak veel groter).
Je kunt dus zeggen dat 99,9 procent van de zonne-energie die de aarde bereikt niet gebruikt wordt door planten. Dat deel van de energie gaat op andere manieren door het systeem van Gaia, zoals in het aandrijven van de waterkringloop. Hoe dat zit valt buiten het bestek van dit artikel.
Hiermee besluiten we wat Tyler Volk ons te vertellen heeft, maar is het onderwerp ‘fotosynthese’ nog niet afgehandeld.

Ruim twintig jaar na Volk beschrijft Gemma Venhuizen in de NRC van 11 juli 2020 ‘Het rommelige proces van de fotosynthese’.* De reactorcentra heten hier PS2 (voor het invangen van zonlicht) en PS1 (voor de productie van koolhydraten).
Huub de Groot, hoogleraar biofysische organische chemie, vat in dit artikel het hele fotosyntheseproces nog eens samen in vier stappen. Allereerst wordt (…) de energie van de fotonen overgedragen aan PS2. (…) In stap twee vindt er scheiding van elektrische ladingen plaats: chlorofyl geeft een negatief geladen elektron af, waardoor positieve lading overblijft. En dat is belangrijk voor stap drie: de watersplitsing. ‘Met behulp van de positieve ladingen worden watermoleculen gesplitst in waterstofionen en zuurstof: zo komen we aan de ‘O₂’ in de fotosyntheseformule.’ De afgestoten negatieve elektronen en de waterstofionen vervullen tegelijkertijd ook een belangrijke functie: zij worden naar PS1 getransporteerd, waar onder invloed van nog meer fotonen en van de moleculen ATP en NADPH de productie van koolhydraten plaatsvindt met kooldioxide.’
Vanwege de sleutelrol die fotosynthese in de natuur speelt willen onderzoekers begrijpen hoe het werkt. Dankzij inzichten die ze opdoen hopen biologen als Jeremy Harbinson, hoofddocent aan de WUR, en Ronald Pierik, hoogleraar fotobiologie van planten in Utrecht, het proces in planten te kunnen optimaliseren. Gunstig voor de plant, die dan minder energie verbruikt, maar óók voor de mens, die zo profiteert van grotere of sneller groeiende gewassen.*
‘Bij elke stap in de natuurlijke fotosynthese gaat kostbare energie verloren’, zegt Pierik. ‘Goed beschouwd is het helemaal niet zo’n efficiënt proces.’ Een van de limiterende factoren is het enzym Rubisco. (…) De inefficiëntie van Rubisco zit ’m erin dat er in pakweg één op de drie reacties van het enzym geen carboxylatie plaatsvindt – maar oxidatie. (Dat werd behandeld in aflevering 10.)
Dat ongewenste bijeffect stamt vermoedelijk uit de tijd dat er nog helemaal geen zuurstof in de atmosfeer zat, legt Roberta Croce uit. Zij is hoogleraar biofysica van fotosynthese aan de Vrije Universiteit in Amsterdam, en houdt zich net als Huub de Groot bezig met de meer fundamentele kanten van het proces.* (…) Het proces is [door de zuurstoftoevoeging in de atmosfeer] door de tijd heen inefficiënter geworden. ‘Nu wordt pakweg 1 procent van het inkomende licht vastgelegd als energie. Ontzettend weinig. In onze vakgroep proberen we onder andere de absorptie van ver-rood licht met golflengtes boven de 700 nanometer te vergroten. Dat doen we door chlorofyl uit cyanobacteriën – die heel goed zijn in die specifieke absorptie – in de planten aan te brengen.’ Zo ontstaan er dus planten met bacterie-dna.
Croce is in het bijzonder geïnteresseerd in de lichtreacties. ‘In principe is het een goed geolied systeem, maar het lastige is dat PS2 en PS1 niet altijd goed samenwerken. Dat kan onder andere voor problemen zorgen als planten te veel licht krijgen, of juist te weinig.’ Belangrijk daarbij is dat beide fotosystemen voldoende licht krijgen. PS2 absorbeert vooral blauw licht, en PS1 juist ver-rood. Een plant in de volle zon vangt licht van het gehele spectrum op, maar in de schaduw is er vooral veel ver-rood licht. ‘Dan kan het dus gebeuren dat PS1 wel genoeg licht ontvangt, maar dat er geen elektronen binnenkomen vanuit PS2 omdat er te veel schaduw is.’ Daaraan kunnen planten zich nog wel binnen een paar minuten aanpassen door de elektronen te herdistribueren.
Andersom kan het voorkomen dat een plant teveel licht krijgt. Dat is ook nadelig, omdat de bladeren kunnen verbranden én omdat er teveel vrije elektronen zijn die schade kunnen aanrichten in het weefsel van de plant. In zo’n geval moet de absorptie van fotonen worden geminimaliseerd, maar dat zou te lang duren en daarom activeert de plant een snel proces dat een groot deel van de geabsorbeerde energie weggooit. Dat proces is lastig stop te zetten – zelfs als de plant weer in de schaduw staat gooit hij nog veel energie weg.
(Denk hierbij ook aan het onderscheid van ‘bespaar’ tegenover ‘vernieuw’ van Charles C. Mann in zijn boek De tovenaar en de profeet.)
Het is niet verbazingwekkend dat onderzoekers nieuwsgierig zijn, wel met welke blik ze tegen de fotosynthese aankijken: planten moeten tot de menselijke orde worden geroepen. En er is meer in dit NRC-artikel.

‘De hoeveelheid licht die een plant opvangt, is van heel veel factoren afhankelijk’, zegt Pierik. ‘Het tijdstip op de dag, het seizoen, de aanwezigheid van buurplanten… Zelfs als de wind door de vegetatie waait treden er al fluctuaties in beschaduwing op.’ In de bladeren zelf speelt de plek van de bladgroenkorrels een rol: die kunnen zich op elkaar stapelen (bij teveel licht) of zich juist over het blad verspreiden (in de schaduw).
Doordat er bij fotosynthese zoveel verschillende eiwitten betrokken zijn, bestaat er ook geen speciaal fotosynthese-gen – die eigenschap is verdeeld over een heleboel afzonderlijke genen. ‘Door op die genen te selecteren, hopen de onderzoekers gewassen te kweken die goed zijn in fotosynthese en zo een hogere opbrengst genereren’, zegt de Wageningse hoogleraar erfelijkheidsleer Mark Aarts. ‘We proberen nu te begrijpen waarom de ene plant zoveel efficiënter is in het fotosyntheseproces dan de andere. Zowel bínnen soorten als tussen soorten zien we verschillen.’
Hoofddocent aan de WUR, de bioloog Harbinson zegt: ‘In principe zijn alle plantensoorten ertoe in staat. Maar voor sommige planten zijn de kosten mogelijk te hoog om in goede fotosynthese te investeren.’ Bijvoorbeeld op een locatie met veel verschillende plantensoorten, en weinig beschikbare stikstof en fosfaat in de bodem. Fosfaat hebben planten onder andere nodig voor ATP-moleculen, en stikstof voor Rubisco. ‘In zo’n geval kan het energiezuiniger zijn om te beknibbelen op fotosynthese dan om de concurrentie aan te gaan met andere planten om schaarse voedingsstoffen.
De ‘normale’ fotosynthese is de C3-fotosynthese, waarbij het eerste tussenproduct een koolstofzuur met drie koolstofatomen is. Die vorm vind je terug bij zo’n 95 procent van alle planten. Daarnaast bestaat er ook een turbovariant, de C4-fotosynthese, met een soort toegevoegde koolstofpomp die de kooldioxideconcentratie in het blad zodanig verhoogt dat [de tegenwerking van] zuurstof vrijwel geen kans meer krijgt. Daardoor vindt er minder fotorespiratie plaats, en kan de plant meer kooldioxide omzetten in glucose. Nadeel is dat dit systeem natuurlijk óók energie kost.’
‘Voor planten is het in theorie gunstig dat de kooldioxideniveaus in de atmosfeer stijgen’, zegt Harbinson. ‘Maar in de praktijk niet per se. Ten eerste is de kooldioxideconcentratie op zichzelf dus niet de enige factor die bepaalt hoe efficiënt de fotosynthese verloopt. En ten tweede zorgt opwarming ook voor nadelen, zoals droogte en hitte-stress – die belemmeren de planten juist.’
Aarts vult aan: ‘Planten kunnen natuurlijk niet weg van hun plek – dat hóéft ook niet, omdat ze hun voedsel uit zonlicht halen en met de energie daaruit verdedigingsmechanismen kunnen maken: gifstoffen, doorns… Maar ze kunnen zich niet een-twee-drie aanpassen aan klimaatverandering, of ingrijpende wijzigingen in hun leefgebied. Terwijl ze zo’n centrale rol vervullen in ecosystemen. Dankzij hén hebben we voedsel en zuurstof. Fotosynthese is letterlijk een proces van levensbelang.’ (Hier eindigt dit NRC-artikel.)
En dan nog deze aanvulling uit een ander NRC-artikel: Tabaksplanten waarbij de stofwisseling genetisch ingrijpend is gereorganiseerd, groeien stukken harder dan hun wilde soortgenoten. Het drooggewicht van de aangepaste planten ligt tot 40 procent hoger. Dat blijkt uit onderzoek van vier plantwetenschappers van de universiteit van Illinois.*
Landbouwwetenschappers zien de C3-methode als een verkwistend proces. Zo ook deze onderzoekers. Ze manipuleerden tabaksplanten op drie manieren, met genen van ofwel de bacterie E. coli, ofwel pompoen en zandraket, ofwel pompoen en een alg. Veel van de ingrepen waren gericht op het molecuul glycolaat, een tussenproduct dat in C3-planten bij fotosynthese ontstaat in de chloroplasten (bladgroenkorrels), en van daaruit wordt vervoerd naar andere orgaantjes (de peroxisomen) waar het wordt omgezet in kooldioxide. De extra ingebrachte genen zorgden ervoor dat glycolaat in de chloroplasten blijft. Eerst werden proeven in de kas uitgevoerd, daarna in het veld. Bij de groep tabaksplanten met genen van pompoen en alg zagen de onderzoekers de meeste gewichtstoename, tot 40 procent vergeleken met wilde soortgenoten. De volgende stap is die gewichtstoename gericht te sturen naar de gewenste plantdelen, zoals het blad of de stengel.
Dit is dus de uitgangssituatie voor de planten, maar ook voor de boeren. Nu over naar het samenleven van planten in de natuur: successie.

In zijn boek Vanuit de plant gezien beschrijft de bioloog Arjen Mulder wat er gebeurt als aan de vloedlijn een kale strandvlakte voor planten voor het grijpen ligt.* Mulder permitteert zich hierbij wel enige dichterlijke en antropocentrische vrijheden. Zo geeft hij biestarwegras een wel erg ‘nobele’ rol. Bij het verband dat gelegd wordt tussen biestarwegras en de aminozuren uit zeesterren, of het zich voeden van helm met verteerd biestarwegras worden stappen overgeslagen. Helm is autotroof, het gebruikt hoogstens de mineralen uit die afbraakresten, dus is de link van het woord ‘voeden’ naar heterotroof ‘eten’ verwarrend.* Maar omdat het verhaal beeldend beklijft, neem ik het toch letterlijk op:
‘Achter de gladde meters [vanaf de vloedlijn] verschijnen de eerste ribbels in het zand, een paar centimeter hoog. … Nog een eindje verder weet zich een plantje te handhaven op zo’n richel, een op het zand opvallend groen maar verder onooglijk graspolletje. Het tooit zich met de naam biestarwegras. Het is een directe verwant van de tarwe, die de mensheid haar dagelijkse brood en gluten levert, en in de volle zon rolt het plantje zijn lange smalle bladeren op als een bies. Is de lucht vochtig, dan spreidt het ze in de lancetvorm van een grasblaadje. De stengel is taai, het blad slap en buigzaam. De bloeiwijze is een stevige tarweaar die uit het naakte zand oprijst en lichtbruin afsteekt tegen het geel van de uiterste strandrand. Dit is het begin van de duinen.
Het zaad van biestarwegras kiemt alleen in zoet water. Wanneer een richel opstuift, komt het fijnste zand vanzelf boven te liggen, terwijl het zwaardere en grovere zand naar beneden rolt en zichzelf uitsorteert. Omdat de zandkorrels in de richeltop zo klein zijn, ontstaat er een capillaire werking die zoet water vasthoudt, want zout water is zwaarder en zakt met de grotere zandkorrels omlaag. Na een regenbui blijft er zoet water in de richelrand achter en als het biestarwegraszaad nu maar snel genoeg kiemt, heeft het al zo veel wortels en bladeren gevormd wanneer bijtend zout aanwaait vanaf de stuivende branding, dat het deze aanval met een glimlach doorstaat.
De wortels van het biestarwegras groeien vanuit een centrale hoofdas in etages onder elkaar tot ongeveer tien centimeter diepte. Zo leggen ze de zandkorrels vast en blijven de wortels in de zandlaag zitten waarin het zoutgehalte van het zeewater tot precies twee derde is verdund. Een beetje regenwater moet doordruppelen in het diepere zoute zand, maar niet te veel. Deze groei-eis van biestarwegras is streng voor een milieu met zo’n wisselend zoutgehalte, maar als het grasje eenmaal aanslaat, maakt het zelf de zandrichel waar het op groeit hoger met zijn stengel en bladeren. Daar begint zich dan weer fijn zand achter op te hopen. De verhoging van de richel verplicht het biestarwegras steeds weer een hogere etage van zijn wortelstelsel aan te leggen om de juiste positie in de zoutgradiënt te behouden. In een jaar of vier groeit zo het oorspronkelijke richeltje tot een protoduin van zo’n twintig centimeter hoog.
Biestarwegras is de stichter van Nederland. Het verovert land op de zee en schept leefbare grond in de moordende leegte van de anorganische krachten. Het vervult zo een heroïsche rol, maar eerder uit een schelmenroman dan uit een koningsmythe. Het strijdt niet tragisch tegen de zee en haar eeuwige macht, maar maakt listig gebruik van de natuurkundige krachten op zijn groeiplek om een Wohnhülle te creëren van alleen maar zand, wortels en een paar blaadjes. Biestarwegras is als enige plant in de wijde omtrek in staat het strand te koloniseren. De zandrichels worden het hoogst als ze aanslibben op oude vloedmerken waarin bruinwieren, schelpdieren en een enkele zeester liggen te rotten. Hier sijpelen fosfaten, nitraten en aminozuren uit, en die zuigt het biestarwegras op via zijn wortels om er de eiwitten in zijn cellen mee te bouwen.
Doordat biestarwegras alleen het fijnste, capillaire zand vastlegt, formeert zich laag op laag een steeds bredere bel zoet water in de steeds hogere zandrichel, die nu al een klein duin kan worden genoemd. Daarop vestigt zich na een jaar of wat het stevige helmgras. Het zaad daarvan kan net als dat van biestarwegras alleen ontkiemen in zoet water, maar anders als dat van zijn voorganger heeft helm voor haar verdere groei juist geen verdund zeewater nodig, maar alleen zuiver zoet water, en dit vinden haar wortels in het steeds hoger wordende biestarwegrasduintje. Helm is een strenge grassoort. De stijve, puntige bladeren vormen een gesloten buis die niet meer open kan vouwen. De bloeiwijze is geen aar maar een volle zwiepende pluim. Helm heeft een veel groter zandvangend vermogen dan biestarwegras, dus de duintjes met helm worden hoger en hoger. Het wortelstelsel van helm is een woest netwerk dat zandlagen van meters naar alle kanten doorboort en vastlegt. De wortels voeden zich met de verteerde resten van het ondergestoven biestarwegras.
Helm verdringt biestarwegras, zeggen ecologen. In werkelijkheid heeft het biestarwegras de levenscondities voor de helm geschapen.

En kijk daar, op beschutte plekken tussen de keiharde helmpollen schiet een kekke, struikachtige plant op met bijna lichtgevend geelgroene lovertjes, de heksenkleur van zeewolfsmelk. De plant heeft een ingewikkelde, materieverslindende opbouw van kaarsrechte stengels met dicht opeengepakte, langwerpig ronde bladeren, die opvallend verticaal gericht staan. De bloempartijen aan de top van de stengels staan als groepjes parasollen naast elkaar. Zeewolfsmelk vindt alleen genoeg bouwstoffen voor haar eiwitten als ze haar lange wortels de diepte in boort en alle voeding aanzuigt die ze kan vinden in begraven, rottende algen en ander organisch afval dat hier ooit is aangespoeld. De zeewolfsmelk wijst op een oud vloedmerk diep onder het zand. Waar nu een duinpartij rust, spoelde twintig jaar geleden de zee nog.
Hier kronkelt over het zand het dikke lichaam van de zeeraket met haar mosterdscherp smakende blaadjes en haar zacht paarsroze kruisbloempjes. De eerste leden van een plantengemeenschap melden zich in de door helm gecreëerde zandrust. Aan de luwe kant van het duin steekt de blauwe zeedistel haar stekelbladeren in de hoogte, blauw vanbuiten, groen vanbinnen. Blauw beschermt tegen de felle, muterende ultraviolette straling op deze schaduwloze plek. Tussen de distels duwen zandhaver en zandzegge hun ondergrondse wortelstokken door het zand en leggen het voorgoed vast in een zandlichaam. Zeemelkdistel, zeewinde, duinriet… het kan niet meer op in de nieuw ontstane vegetatie.
In de beschutting daarvan slaan duindoorns aan. Zij vormen struwelen die alle eerdere planten overwoekeren en wel vijf meter hoog worden. De kracht van duindoornstruiken is dat ze aan hun wortels knikkergrote knolletjes hebben met daarin bacteriën uit het geslacht Frankia. Deze ademen stikstofgas uit de lucht en leggen die vast in nitraten en nitrieten en staan die af aan de plant, die er eiwitten mee aanmaakt. De noeste duindoorn voegt via haar knolletjes stikstofrijk voedsel toe aan het überschrale duinmilieu. Er zijn nu amper beperkingen meer aan haar groei en er zouden massieve bestanden van hoge duindoornstruiken verrijzen – bunkers met zilveren schubben – als niet ook de vlier zich er nu kon vestigen als gevolg van de stikstofverrijking van de bodem. De wilde vlierstruik groeit tot boomhoogte uit en zet met zijn grote gedeelde bladeren die duindoorn in de schaduw. Datzelfde doen de elzen die zich langs een duinwatertje vestigen. Net zoals de duindoorn hebben ook elzen wortelknollen, vuistgrote, met al even actieve Frankia-bacteriën. Door de afwisseling van struik en boom ontstaat er toch weer variatie in het beginnende binnenduinbos.
Verderop wordt het landschap beheerd. Opschietende duindoorns en andere struiken worden jaarlijks gerooid en de bodem eens in de tien jaar volledig afgeplagd. In de kunstmatig opengehouden duinvallei verschijnt spontaan een plantengemeenschap van wel 150 soorten die elders vaak uiterst zeldzaam zijn. Een duinmeer loopt vol met schoon kwelwater, opgestuwd door de waterbel die vastligt in de zeereep en de hogere duinen. Langs het open water ontstaat een dicht gazon vol botanische parels. Rond wintergroen. Breedbladige wespenorchis. Rode ogentroost. Witte honingklaver. Honingorchis. Moeraskartelblad. Waternavel. Duizendguldenkruid. Vleugeltjesbloem. En de jonkvrouw in de bonte massa, parnassia, met haar hoge, witte, vijftallige bloemen. Het milieu is een lappendeken van microklimaten en -niches die verschillen in hun gehalte aan zout en mineralen, kalk, nitraat, fosfaat, merendeels uit konijnenplas. Wind, regen, zee en dieren zorgen voor constante dynamiek. De planten houden de bodem vast, maar veranderen ook de samenstelling ervan, want plantenwortels scheiden zuur uit en daarin lost kalk op.
Dat niet alle stikstof hetzelfde is, lezen we verderop in aflevering 37 van dit artikel.

Wat begon als een door zee, zout en wind kaalgebeukte strandvlakte met wat zandrimpels en slechts één plantensoort, het bewonderenswaardige biestarwegras, is vijftig meter landinwaarts veranderd in ofwel een gesloten soortenarm bosstruweel, ofwel een open, soortenrijke duinvallei. Successie heet het ontwikkelingsproces dat voert van enkele pioniersplantjes naar een al dan niet door mensen in stand gehouden climaxsituatie. Successie is een verschijnsel in ruimte en tijd. De eerste [soorten] zijn altijd klein en sterk, taai en listig. De laatste zijn het hoogst en leven het langst. De successie begint in Nederland met een grasje en ontwikkelt zich in de loop van tientallen jaren spontaan tot een beukenbos. Daarna stopt de successie en spreekt men van een climax.
Successie kan twee kanten op: langs een opbouw- en een degradatiecurve. Als de situatie ter plekke verslechtert, sterven als eerste alle bomen nabij de bron van de ellende, de dennen eerst, de loofbomen later. Daarna verdwijnen na elkaar de hoge struiken, de lage struiken, de kruidachtige gewassen, de mossen en tot slot de uiterst taaie korstmossen. Kale grond blijft over. De ‘universele verschralingsgradiënt’ is ook te volgen naar de koude polen toe en tegen bergen op. Dezelfde graduele ondergang van bossen naar lagere vegetaties naar grasland en ten slotte dode woestijn zet wereldwijd door als gevolg van de opwarming van de aarde.
Bos is het natuurlijk eindpunt van de successie in heel Europa en ook een groot deel van de tropen. In een ecologische climax kan het soortenbestand in principe voorgoed hetzelfde blijven, zolang de omstandigheden maar niet radicaal wijzigen door een klimaatverandering, langdurige overstroming of een ruimteverslindende invasieve exoot (zoals de mens). Ecologen noemen een climaxvegetatie liever ‘rijp’, of gewoon ‘oud’. (Hierachter zit bij Arjen Mulder een visie die gedateerd is. Over de vier ecologische stromingen die onderscheiden worden, gaat een apart intermezzo op Ecopedia.)
De climaxsituatie is niet de natuur op haar best. Er leeft niet het maximaal mogelijke aantal soorten in één gebied. Het grootste soortenaantal wordt bereikt kort voor de climax zich instelt. Daarna loopt het aantal wat terug en blijft lang, heel lang hetzelfde. Een climaxvegetatie met een levensduur van twintig miljoen jaar is geen uitzondering. In Nederland is de climax overal het beukenbos, behalve in de resterende moerassen, waar uiteindelijk elzenbroekbos ontstaat. De open duinen zijn het meest veranderlijke landschapstype van Nederland. Toch zou het ook hier dichtgroeien met bos als vlijtige beheerders en vrijwilligers de gronden niet maaiden en het maaisel afvoerden. Zij handhaven de voedselarmoede uit het begin van de successie die voor de meeste duinsoorten onmisbaar is.
Successie leidt tot de vorming van een biocoenose. Soorten creëren de milieucondities waarin andere soorten kunnen floreren. Steeds weer vestigen planten zich in een karig milieu en maken er een voedselrijkere groeiplaats van, waar andere planten kunnen gaan bloeien. Op hun beurt wijzigen deze de omstandigheden zo dat de eerdere planten het er niet meer uithouden en op zoek gaan naar een kariger milieu elders.
Successie houdt pionierplanten actief en in beweging. Dit garandeert dat alle kale grond overal begroeid raakt, zonder dat er een mens hoeft te helpen. Ook climaxsoorten hebben geen hulp nodig, want zij werken met elkaar samen, en met ontelbare microben, schimmels en fiks wat dieren: bodemkruipers scheppen luchtigheid rond hun wortels, insecten bestuiven hun bloemen en eekhoorns en gaaien planten hun zaad voort. Laat je in Nederland de natuur haar gang gaan, dan zou het soortenaantal teruglopen tot een stuk of vijftig plantensoorten in een rijp, licht gevarieerd beukenbos en misschien nog eens zoveel in een verland veenmosmoeras.’
Hiermee eindigt het verhaal van Arjen Mulder. Precies zijn laatste bewering gaan we (successievelijk) kritisch tegen het licht houden.
Successie wordt op 4eco door Owen behandeld in aflevering 54 van artikel 3 uit de serie ‘Wat is ecologie?’ in de rubriek Ecologie en in de aanvulling op Owen ook in aflevering 84. De climax komt daar al eerder aan de orde in aflevering 37.
Het creëren van milieucondities lijkt mij een voorbeeld van ontwikkeling dat aan de orde kwam in aflevering 1. Over microben en ander bodemleven gaat het verderop in dit artikel vanaf aflevering 30.
In de afleveringen 18-22 bekijken wat de Amerikaanse hoogleraar ecologie William Drury in zijn Angelsaksische situatie te zeggen heeft over successie, maar lees misschien beter eerst het intermezzo over ecologische stromingen op Ecopedia.

Hoe kwam de theorie van successie tot stand en hoe stevig staat hij in zijn schoenen? De Amerikaanse hoogleraar ecologie William Drury had in de vorige eeuw grote twijfels bij het toen gangbare beeld (dat heerste in de academische gemeenschap aan de overkant van de oceaan). We laten hem hier aan het woord tot en met aflevering 22:*
Drury benoemt in dit verband om te beginnen drie begrippen uit de Griekse filosofie van Aristoteles.* Namelijk het concept van de microcosmos/macrocosmos dat zegt dat de interne organisatie van een onderdeel de organisatie van het geheel na-aapt, wat meebrengt dat onderdelen van een groot systeem op zichzelf zouden moeten staan.* Dan is er het concept van de ‘Great Chain of Being’, de Scala Naturae, ook wel vertaald als de ladder van de natuur. In de vorm van een progressie van imperfectie naar perfectie leverde dit een scheiding op tussen ‘lagere’ en ‘hogere’ vormen van leven. En als derde is er het concept van evenwicht in de natuur.
Drury zag deze filosofische concepten terug in de ecologische theorie. Het laatste idee, dat van evenwicht in de natuur, spreekt uit het bijna alom aanwezige gebruik in de ecologie van evenwichtsmodellen voor levensgemeenschappen in de natuur.
Wat een ‘levensgemeenschap’ is werd (in Amerika) voor het eerst geformuleerd door Forbes: ‘Het meer is een oud en tamelijk primitief systeem, afgezonderd van zijn omgeving. Erbinnen vind je een kringloop van stof en regelmechanismen zorgen voor een evenwicht dat vergelijkbaar is met een dergelijk gebied op het droge. Deze microcosmos valt niet volkomen te begrijpen tenzij de relatie tot het geheel ervan duidelijk te zien is.’*
In dit citaat (zegt Drury) vallen de woorden ‘afgezonderd’ en ‘evenwicht’ direct op. De gedachte is dat het begrijpen van de microcosmos (de levensgemeenschap) van het meer een begrip oplevert van de macrocosmos van de wijdere wereld. Als de een in evenwicht is, wordt verwacht dat de ander dat ook is. Zo werden twee principes van Aristoteles – de micro/macrocosmos en het evenwicht van de natuur – opgenomen in het ecologische bevelschrift.
Halverwege de vorige eeuw schrijft een studieboek: ‘De levensgemeenschap handhaaft een zeker evenwicht, stelt een biotische grens in en kent een zekere eenheid die gelijk oploopt met het dynamische evenwicht en de organisatie van andere levende systemen. Natuurlijke selectie werkt in op het algehele onderlinge soortensysteem, wat leidt tot een langzame evolutie van integrerende aanpassing en evenwicht.’* Hier hebben we de Scala Naturae. We zien hier ook een nadruk op een onderscheiding in onderdelen zowel als een intern gehandhaafd evenwicht.
De levensgemeenschap werd in de ecologie zo een samenstel waarin de onderdelen (de soorten) door ruimte en tijd heen met elkaar verbonden kunnen worden en dat zelf ook qua veranderingen door de tijd heen te volgen is. Daarbij werd het woord successie gebruikt. Dat gaf de progressieve vervanging van levensgemeenschappen weer, de stap-voor-stap voorbereiding van een plaats voor de vegetatie van het volgende stadium [en natuurlijk voor dieren, schimmels en microben, zou ik hier aan toe willen voegen], en het behalen van een vooraf vaststaand eindpunt dat bepaald werd door het heersende klimaat. Dat eindpunt is de ‘climax’ die verondersteld werd in stand te blijven totdat hij vernietigd werd door een of andere verstoring.
Men zag dit voor zich: een progressieve ontwikkeling van de bodem; toenemende stratificatie in de plantengemeenschap; een toenemende voorraad anorganische voedingsstoffen vastgelegd in het plantenweefsel; toenemende productiviteit; de levensgemeenschap die het lokale microklimaat gaat bepalen; toenemende soortenrijkdom; een afnemende verdringing van soorten; en een toegenomen stabiliteit. Al deze ‘trends, of progressieve ontwikkelingen’ zijn belangrijke uitgangspunten die aan de basis liggen van de conventionele ecologie.
Wie wil weten welke ideeën hierover in Europa heersten, kan dat lezen in het in de noot bij aflevering 13 genoemde proefschrift ‘Scheidslijnen in het denken over natuurbeheer in Nederland’ van Mechtild de Jong.

‘Hoe stevig staat de theorie van successie in zijn schoenen?’ vraagt William Drury zich dus af. Het viel hem op dat botanici die de vegetatie beschrijven wel wat weg hebben van impressionistische schilders. Om met anderen te communiceren moeten ze hun waarnemingen precies vastleggen en creatieve verbeelding toepassen om ze te verklaren. Wie een landschap bestudeerd wil het gewone erin beschrijven. Waarnemers, of het nu wetenschappers of schilders zijn, ontkomen er niet aan dat hen bepaalde kenmerken opvallen ten koste van andere. Waar de kunstenaar dit juist aanmoedigt, probeert de wetenschapper dit te onderdrukken, maar de persoonlijke reactie blijft bestaan. De vegetatie is niet het equivalent van de lijst van plantensoorten van een gebied (dat is de flora). De vegetatie is opgebouwd met combinaties van plantensoorten (levensgemeenschappen). De visuele en biologische impact ervan wordt grotendeels betaald door de relatieve rijkdom en overheersing van de grootste en meest in het oog springende planten.
Botanici concluderen vaak als vanzelf dat in het oog springende soorten een belangrijke rol spelen in de ‘gemeenschap’ die zij beschrijven. Aldus valt een strook bloeiende struiken langs de rand van een plas hen op, en een moerasbosje in een duinholte, of een rijtje berken op een stenige helling. Het gevaar van persoonlijke reacties wordt duidelijk wanneer ecologen zich gaan bezighouden met gekunstelde abstracties. De meesten nemen aan dat de eenheden die zij beschrijven als gemeenschappen fungeren, alsof elke soort die er is, co-existeert met waar het oog van de ecoloog op valt.
Mensen hebben sterk de neiging om stereotypen te creëren, ‘typische vormen’ en de variatie in de natuur daaraan te koppelen. Neem het stereotype ‘eikenblad’. De bladeren van een enkele eik verschillen onderling al sterk in vorm en grootte en de bladeren van elke eikensoort verschillen opvallend met die van de twaalf andere soorten van het noordoosten van Amerika. Ik kan, zegt Drury (want hij tekent zelf), dertig of veertig bladeren bekijken en dan een tekening van één blad maken die de ‘rode eikheid’ weergeeft, in tegenstelling tot de ‘zwarte eikheid’ (of nog een andere eikensoort). ‘Ik kan het’, zei een bevriende botanist, ‘meer op een rode eik laten lijken dat in het echt.’
Het is maar al te gemakkelijk om dit proces toe te passen op vegetatie, om in gedachten een beeld te scheppen van wat ‘typisch’ is en dat op vegetatie-eenheden in het landschap te plakken.
Als ik de kenmerken van de plantensoorten in deze eenheden inventariseer, zegt Drury, vind ik een paar algemene en in het oog springende soorten die samen voorkomen. Die vormen het ‘struikgewas’ in de drassige laagtes, de ‘weiden’ langs een kreek, de ‘dennenbosjes’ op het zand, en de ‘heide’ op de arme gronden. Botanici noemen deze soorten dominant of primair. Samen met de in het oog springende soorten, komen andere, minder opvallende soorten voor, de zogenaamde secundaire soorten. Naarmate je meer terrein bestrijkt wordt de lijst van secundaire soorten langer en langer. De primaire soorten bepalen de ‘eenheden’ van de waarnemer, ook al kunnen de onopvallende soorten talrijker zijn.
Dit maakt duidelijk dat je heel gemakkelijk vertrouwd raakt met je eigen idee van een bepaalde plantengemeenschap, schrijft Drury, en dat je dan de steekproeven negeert die botsen met dat stereotype – hoe veelvuldig die afwijkingen ook voorkomen. Als je daaraan toevoegt dat de meesten van ons hun vermogen om patronen te zien die anderen missen, hoog hebben zitten, dan creëer je een vak dat veel weg heeft van impressionistisch schilderen.
We moeten niet kijken naar hoe het in de natuur volgens onze (deterministische) modellen zou moeten zijn, maar waarnemen hoe het is. En dan geldt dat toeval en verandering overheersen. De toekomst is voor andere organismen net zo onvoorspelbaar als voor ons. Verstoring komt te vaak voor om je op evenwicht in te stellen. Individuele organismen kunnen zich in het licht van een onzekere toekomst geen consistentie veroorloven. Ouders die uiteenlopende nakomelingen voortbrengen zullen gemiddeld gesproken in de volgende generatie beter vertegenwoordigd zijn dan ouders die uniforme groepen jongen voortbrengen.* En veel jongen is beter dan weinig.
We gaan nu over naar een voorbeeld.

Na de afloop van de laatste ijstijd, zo’n 12.000 jaar geleden, werden door zeestromingen langs de Amerikaanse kust enorme massa’s zand verplaatst. Soms blokkeerde dat de monding van een rivier. En wanneer die rivier afgeremd werd, daalde het meegevoerde fijnkorrelige materiaal in de beschutte ruimte achter de blokkade neer. Dit sediment vormde dan modder- en zandvlaktes. We volgen nu de beschrijving van Drury van wat daar vervolgens gebeurde. In het kort komt het er op neer dat zoutminnende grassen de vlakte koloniseren en dat er zich afzettingen van zilt ‘veen’ vormen.
Het patroon van hoe plantensoorten over een kwelder verdeeld raken volgt grofweg wat je theoretisch mag verwachten. Aan de zeezijde vind je in Amerika een bijna zuivere opgroei van slijkgras. Er zijn twee soorten van, met de Latijnse namen Spartina alterniflora en Spartina patens. In het Engels zijn hun namen verschillend: thatch en marsh hay, in het Nederlands niet. Vandaar dat ik ze hier onderscheid met ‘laagtij’ en ‘hoogtij’ ervoor. Je hebt dus laagtij-slijkgras – dat zich direct al vestigt – en hoogtij-slijkgras, dat tot koloniseren in staat is wanneer het gebied twee derde van de tijd met vloed niet meer onderloopt.
Laagtij-slijkgras kan een langere onderdompeling in zeewater verdragen omdat het zoutafscheidende klieren op het oppervlak van zijn stengels en bladeren heeft. Net zo belangrijk is dat het de snelle sedimentatie overleeft, die de uiteinden van delta’s (van New England, de regio in het noordoosten) gedurende duizenden jaren kenmerkte.
Als het slijkgras zich eenmaal vestigt, beïnvloeden de stengels en bladeren de stroming van het modderige water aan de mond van de rivier. Echt darmwier, een groene alg, groeit op de modder en de grasstengels en vangt het sediment af. Dan, wanneer silthoudend* zoet rivierwater zout zeewater treft, vindt er een natuurkundige wisselwerking plaats die zorgt voor verklontering in fijne afzettingen en zodoende voor snelle aangroei. Eenmaal gesetteld kleven silt en klei, eveneens door natuurkundige oorzaken, aan de modder die er al ligt en laten zich niet zomaar weer in suspensie spoelen. Met de aanwas van de sedimenten, stijgt het niveau van de kwelder. Aan de uiteinden ervan is goed te zien dat het laagtij-slijkgras bezig is de ondiepe zand- en moddervlakten in beslag te nemen. Je ziet het ook langs de oevers van de vele kronkelende stroompjes waar de hogere kwelder op afwatert.
Hoogtij-slijkgras bezet de bovenkant van de kwelder, waar het zeewater alleen nog bij springtij overheen spoelt. Het grensgebied tussen de twee soorten slijkgras kan in licht glooiende gebieden breed zijn, maar het is smal langs de getijdekreken en hun steile goten. De hoge kwelder is rijker aan soorten dan het lagere deel dat aan de open zee grenst.
In de ondiepe poeltjes en waterbekkens, de meeste omrand door schuimachtige algen, vinden we vetachtige planten als zeekraal en waterplanten als spiraalruppia. De oeverwallen van de getijdekreken (waar de modder neerdaalt als de stroming afneemt) zijn begroeit met hoogtij-slijkgras, met hier en daar een kluit zoutgras (een andere inheemse Amerikaanse soort) en moerasvlierstruiken. Op nog hogere gronden, aan de binnenzijde van de kwelder, verandert het aanzicht snel. Daar vinden we veel van het overblijvende kruid zilte rus. Aan de rand vinden we dan weer guldenroede, zeelavendel en ‘New York asters’. Tegen de binnenzijde van de duinen treffen we vaak een slinger wasgagelstruiken aan, een Amerikaanse soort waar muggen beschutting vinden.
Amerikaans onderzoek bracht veel aan het licht over wat er in die kwelders zoal aan plantaardig en dierlijk leven te vinden is, niet alleen over de soorten, maar ook door de exemplaren ervan te tellen en te wegen; dus ook over de lokale ‘economie’.*
Kwelders blijken veel organisch materiaal te produceren. Veel komt van het slijkgras, maar ook van Ruppia occidentalis, een lid van de zeegrasfamilie. Ook algen en kiezelwieren, die korstjes vormen op de sedimenten, leverden een flinke bijdrage.
De Amerikaanse situatie verschilt principieel vast niet veel van die van de lage landen, alleen de soorten zijn er wel anders.

Op andere plaatsen leverden groene algen, zoals zeesla (een meercellig groenwier) en draderige wieren die in de afwateringskanalen en ondiepe poelen leven, het ruwe voedsel voor wenkkrabben, moerasmossels, moerasslakken, borstelwormen en een soort garnalen (Palaemonetes pugio). Deze garnalen kauwen bovendien het slijkgras tot kleine stukjes, waardoor het als bezinksel een voedingsbodem voor bacteriën wordt.
Dan zijn er weer soorten die dit bezinksel inslikken, de bacteriën verteren en het ‘kaf’ weer uitspuwen. Dat doen een heleboel individuen en soorten, want bacteriën vestigen zich steeds opnieuw op bezinksel, groeien aan en worden gegeten. Het zal niet verrassen dat er dan allerlei dieren vanuit het water in de monding de kwelder binnenkomen om er hun voordeel te doen met de aanwezige voedingsstoffen; dat doen ze om te groeien, of aan te sterken om jongen te kunnen krijgen, of aan hun trek te kunnen beginnen.
Als het getij door de zeearmen de geulen instroomt en de kreken van de kwelder bereikt, komen kleine kweldervisjes zoals de Fundulus heteroclitus mee, op zoek naar wormen, garnalen, krabben en wat er daar nog meer van de algen of het organische bezinksel leeft. Deze kweldervisjes en ook krabben trekken op hun beurt roofdieren aan, zoals zeebaars, zeeforel, visdiefje, zaagbek en verschillende soorten reigers. Er is sprake van wat ecologen een voedselketen noemen.
Ten tijde van dit onderzoek, midden vorige eeuw, lag het voor de hand te concluderen dat het laagtij-slijkgras dat opgroeit waar de getijdengeul is – dus aan de voorkant van de aangroeiende kwelder – de wegbereider is van de tweede soort, het hoogtij-slijkgras, met daarop volgend de toenemende soortendiversiteit die op de hoge kwelder de rijpheid van het systeem weerspiegelt. Men was het er indertijd over eens dat de organische elementen, die de ecologen levensgemeenschappen noemden, een samenstel vormden met de anorganische elementen, en zo samen een meer alomvattend systeem opleverden. In de woorden van een toenmalige ecoloog: ‘In een ecosysteem zijn de organismen net als de anorganische factoren componenten die zich in een relatief stabiel dynamisch evenwicht bevinden. Successie en ontwikkeling zijn uitingen van de universele processen die tot het scheppen van zulke in evenwicht zijnde systemen leiden.’*
Je zou dus in die optiek verwachten dat de kwelderbodem uit restanten van laagtij-slijkgras opgebouwd moet zijn, met misschien een toefje hoogtij-slijkgras. Dat zou kloppen met de successietheorie: dat sedimenten en organisch restmateriaal die zich rond laagtij-slijkgras ophopen, de weg bereiden voor de kolonisatie van de kwelder door hoogtij-slijkgras, dat pas verschijnt als het niveau eenmaal dat van het hoogtij bereikt heeft. Het aangehaalde praktijkonderzoek laat echter zien dat het ‘veen’ juist bijna uitsluitend uit hoogtij-slijkgras is opgebouwd, helemaal tot onder in de bodem. En we zien dat veen van laagtij-slijkgras alleen aan de buitenrand van elke veenlaag te vinden is, alsof het louter langs de rand van het veenplateau groeide, net zoals waar we het nu vinden. Wat is hiervoor de verklaring?
Het komt doordat het silt wordt gedeponeerd door overstromingen van het estuarium die de complete bovenkant van de kwelder bestrijken. De zich uitbreidende segmenten van de kwelder zijn kleinschalige delta’s die over hun hele oppervlak sedimenten verzamelen. Die sedimentatie houdt de bovenkant van de delta’s op hoogtijniveau, ook al stijgt de zeespiegel. Dit stelt het hoogtij-slijkgras in staat de bovenkant van de kwelder blijvend te bezetten en geeft de sedimentatie de kans om het opwaarts te blijven aanvullen.
En het laat het oppervlak van de kwelder zich zeewaarts uitbreiden. Met de opbouw van de kwelder door de toevoeging van sediment, beweegt de reikwijdte van het getij, waar het laagtij-slijkgras groeit, weg van de hogere gronden. Zo komt het hoogtij-slijkgrasveen over de afzetting van laagtij-slijkgrasresten heen te liggen. Het laatste ligt dus in een schuine hoek.
De delta is dus niet zomaar een geïsoleerd lokaal verschijnsel. De vorm ervan wordt ook beïnvloed door stromingen en zandverplaatsing in zee, terwijl de hoge productie van het estuarium voortkomt uit het silt dat de rivier meevoert. Die twee voorwaarden komen hier samen.
Het theoretische oordeel wordt dus door praktijkonderzoek onderuit gehaald. Daarom is steeds opnieuw waarnemen zo belangrijk om bij de les te blijven.

Stel je een kaal veld voor dat opnieuw begroeid raakt. De eerste planten die op dat veld verschijnen, zijn kleine, grasachtige, snelgroeiende één- en tweejarige kruiden. Meerjarige kruiden volgen op de eenjarige, waarna struiken de kruiden overwoekeren. Al gauw verschijnen er bomen, waarvan de soort afhangt van de aard van de ondergrond. Tenslotte neemt de zichtbare verandering af en ‘stopt de successie’.
Dat is, zegt Drury, in het superkort wat je vaak leest als successie wordt uitgelegd. Ecologen spreken bij een kaal herbegin van secundaire successie. Zij leggen het als volgt uit: ‘Eén overheersende soort bewerkt de bodem en het microklimaat op zo’n manier dat het de toegang voor een tweede soort vrijmaakt, die overheersend wordt en zijn milieu zodanig bewerkt dat het de eerste soort onderdrukt en de toegang van een derde, overheersende soort mogelijk maakt, die op zijn beurt het milieu verandert.’*
In de vorige eeuw werden in Amerika tal van boerderijen verlaten met kale akkers die als beginpunt fungeerden voor secundaire successie. Zulke plaatsen vormden een prachtig onderzoeksgebied om de theorie te controleren. Dat deed J. McCormick.* Hij schrijft: ‘We haalden van sommige delen van een pas geploegd land eenjarige planten als zaailingen weg, terwijl we die op andere plaatsen wel lieten groeien. De theorie schrijft dan voor dat de eenjarige planten de ‘weg bereiden’ voor de meerjarige planten. Maar tegen het einde van elke zomer waren de meerjarige planten juist meerdere keren zo overvloedig op de plekken waar de eenjarige verwijderd waren. De biomassa (droog gewicht) ervan was er 15 tot 82 zo groot als op de plekken waar de eenjarige nog wel groeiden. Guldenroede, asters, suzanne met de mooie ogen en andere meerjarige planten floreerden op de plekken zonder eenjarige planten, maar deden het totaal niet op plekken met eenjarige.’
Kortom, het klopte totaal niet. McCormick hechtte toen nog zozeer aan de gangbare successietheorie dat hij dit graag als een afwijking wilde beschouwen, niet als een bewijs dat de theorie niet deugt. Dat de theorie echt niet klopt liet Pickett, een andere ecoloog, zien met een langdurig onderzoek.* Hij schrijft:
‘Het land werd in 1960 voor het laatst geploegd en toen aan zijn lot overgelaten. We hebben twintig jaar lang, jaar in jaar uit, de veranderingen in soortensamenstelling en begroeiing gevolgd. De gegevens tonen dat successie individualistisch is, dat wil zeggen samengesteld uit in de tijd breed overlappende populatiecurves. Gedurende het onderzoek vertonen de populatiecurves lange, hardnekkige staarten.* Dat geeft aan dat, over deze periode, successie een proces is waarin soorten die de meeste tijd aanwezig zijn, op verschillende momenten dominant worden. Van buiten binnenkomen en uitsterven zijn niet de leidende mechanismen van verandering in de levensgemeenschap. Bij sommige soorten vielen dubbele of veelvuldige pieken op… Veel soorten die later in de volgorde belangrijk werden, kwamen al vroeg binnen…
…Het patroon van de levensgemeenschap is duidelijk een in de tijd verlopend continuüm, net zoals het te verwachten was… Als je slechts de pieken van de 10 of 12 leidende soorten onderzocht – en dus de kleine aandelen en langere staarten in de curves van de verdeling met andere soorten negeert – zou je tot de beschrijving van groepen kunnen komen die overeenkomt met de overheersende stadia die bij de successietheorie vaak genoemd worden. Onderzoek je echter de totale reeks van soorten en hun complete wisselwerkingen, dan zie je dat het mechanisme van verandering in de levensgemeenschap er níet een is van plotselinge verschuivingen tussen onderscheiden samengestelde levensgemeenschappen.’
Hiermee wordt wel duidelijk dat het idee dat sommige soorten, ten koste van zichzelf, een plek voorbereiden voor andere geen hout snijdt. De meeste soorten zijn er al direct bij het begin. Het gaat er eerder om dat verschillende soorten op verschillende manieren reageren en dat waarop ze reageren van plaats tot plaats steeds weer anders is. De kolonisatie van zo’n kaal terrein demonstreert het enorme potentieel van zaadproductie en van de verspreiding van de betrokken soorten, vindt Drury.
Als zich de gelegenheid voordoet weten vele zich te vestigen, anders sterven ze.

Ik ga nogmaals naar de akker die aan zijn lot wordt overgelaten en kijk wat de Australische bioloog A. Duncan Brown te zeggen heeft over de successie aldaar. Dat haal ik uit zijn boek Feed or Feedback – Agriculture, Population Dynamics and the State of the Planet dat ik in 2003 uitgaf (met de imprint International Books).
De habitat ligt dus klaar om geëxploiteerd te worden en het duurt niet lang voordat de invasie begint. We zien een opeenvolging van verschillende organismen, een successie die gestuurd wordt door een paar eenvoudige maar dwingende principes. De organismen die zich als eersten vestigen komen voort uit de geschiedenis van deze nieuwe habitat. Om te beginnen gaat het om wat wel inocula genoemd worden: zaden, sporen, eieren en levensvatbaar weefsel die uit het verleden zijn overgebleven. Het gaat dan om de afstand die die inocula moeten afleggen, de manieren waarop die afstand overbrugd kunnen worden (wind, vogels, poten, enzovoort) en het type selectie dat door de natuurkundige en scheikundige kenmerken van de nieuwe habitat wordt uitgeoefend.
De kolonisatie van land is zelden zo clichématig als de leerboeken ecologie ons vertellen, zegt ook Duncan Brown. Daar is de norm gewoonlijk dat een successie begint met grassen en andere kleine planten, waarna struikgewas volgt en het eindigt met bomen en volgroeide bossen – als het fysieke milieu de groei van een bos toestaat. Als er veel organisch materiaal uit het vorige regime is overgebleven kunnen de pionierende kolonisten evengoed zogeheten heterotrofen zijn, dat wil zeggen allerlei soorten micro-organismen, schimmels en afvalvreters.* Wanneer die geheel aan hun eigen lot worden overgelaten, gaat het echter net als met de successie van een gesloten systeem, zoals met bacteriën en schimmels bij de kolonisatie van een glas melk. Zo’n ecosysteem draait uit op een sterfhuis en of een slaapstand, tenzij het door planten wordt opengegooid voor de stroom zonne-energie die nodig is om een systeem in stand te houden.
Hebben planten zich eenmaal gevestigd, dan zijn de ruwe morfologische kenmerken van de daarop volgende successie gemakkelijk te zien, hoewel in de meeste gevallen een mensenleeftijd niet lang genoeg is om de waarnemer het proces helemaal tot de volgroeiing, of ‘rijpheid’, te laten volgen. In de vroege stadia zijn de planten klein en met weinig. Met het rijper worden van het systeem neemt de omvang en het aantal van de individuele planten toe. Dit is het patroon, of het systeem in eerdere stadia nu wel of niet gedomineerd wordt door grassen en in latere door bomen. Het komt gewoon doordat volgroeide planten groter zijn dan zaailingen. In het begin is er een heleboel kale grond en de pionierplanten zullen niet gauw last hebben van de schaduw van andere planten, of van ernstige concurrentie om de voedingsstoffen in de bodem. Op enige selectie na die de bodem en het plaatselijke leven uitoefent, hebben de nieuw aangekomenen het in termen van concurrentie vrij gemakkelijk. Dat verandert echter. Het aantal individuele planten groeit aan en er ontstaat concurrentie om voedingsstoffen als de wortels zich zijwaarts en omlaag uitspreiden, en als grotere planten kleinere in de schaduw beginnen te zetten. Dit alles gaat gepaard met het ontstaan van afval en het zich uitspreiden van de wortels, die tezamen de chemie en de structuur van de bodem beginnen te veranderen en in organisch materiaal voorzien dat een groeiende populatie van dieren en microflora onderhoudt. De vestiging van een plantengemeenschap schept natuurlijk ook steeds meer ruimte voor een populatie van herbivoren, die, zij het zonder veel enthousiasme, hun aandeel leveren om ook de carnivoren hun plek te geven.
De voedingspatronen van dieren, of het nu verzamelaars zijn of jagers, zijn verdeeld over de soorten noch allemaal gelijksoortig, noch gelijksoortig destructief. Ze zijn selectief en de consumptie van, bijvoorbeeld, een plantensoort door een herbivoor helpt andere soorten planten direct doordat een concurrent in toom wordt gehouden, en indirect door de voedingsstoffen van de eerste plant, in de vorm van uitwerpselen, door het systeem te verspreiden.
Je kunt deze aflevering ook lezen als een beschrijving van hoe informatie in de loop van de ontwikkeling verandert en dus zelf ook weer het systeem verandert.

Dit alles draait uit op een voortdurende toename in de dichtheid van de biomassa (de biomassa per oppervlakte-eenheid van de grond) en in het aantal soorten. Er komt een tijd, enige eeuwen later, dat de progressie tot een woud leidt, wanneer het systeem zijn ‘climax’ bereikt – een term die hier slaat op een fase waarin een relatief algemene stabiliteit is bereikt. In deze fase zijn er veel soorten en, hoewel er overheersende typen of zelfs overheersende genera kunnen zijn, domineert geen enkele soort in zijn eentje, tenzij het milieu zeer selectief is in de een of andere fysische zin. Hoe complexer het systeem is, hoe groter het aantal soorten. En met meer soorten daalt het aandeel per soort in de totale biomassa. Omdat het beschikbare voedsel voor een dier, de mens meegerekend, zich beperkt tot een gelimiteerd aantal soorten, volgt hieruit dat hoe groter de complexiteit van het milieu is, des te kleiner het aandeel van de totale biomassa is dat voor dat dier ter beschikking staat. Het tropisch regenwoud, het dichtste en meest diverse van alle ecosystemen op deze planeet, kan aldus slechts een kleine menselijke populatie onderhouden. Het is dus niet verrassend dat de mens, voordat er landbouw was, beter gedijde in de open, gematigde bossen en grasvlaktes dan in de jungle. In een onverstoorde jungle vind je geen uitbarstingen van het aantal konijnen, muizen, sprinkhanen – of mensen.
Het rijpe systeem heeft een uitgesproken vermogen tot zelfregulatie, met homeostase als resultaat – het is er bijna een synoniem voor. Dit is in essentie het onderhouden van een tamelijk constante soortensamenstelling, biomassa, energiestroom, omzetting van voedingsstoffen, enzovoort. Vanwege zijn relatieve stabiliteit wordt een ecosysteem op zijn climax door ecologen vaak omschreven als ‘zijnde in een staat van evenwicht’ of in ‘dynamisch evenwicht’. Niets kan verder van de waarheid zijn. Als de term ‘evenwicht’ in een wetenschappelijke context al iets te betekenen heeft, dan moet die betekenis zijn wortels hebben in de thermodynamica. En een systeem in thermodynamisch evenwicht zit op het laagste beschikbare energieniveau in de heersende omstandigheden. Een ecosysteem in evenwicht zou dan bestaan uit dode en/of in rust zijnde organismen. De relatieve constantheid van een volgroeid woud benadert juist het dichtst die van een ‘steady state’, in zoverre het een grote energie-inhoud heeft en haar dynamiek worden onderhouden door een stroom van (zonne-)energie. Er is nog een belangrijk verschil tussen een reactiesysteem in evenwicht en een in steady state; het eerste is vrijelijk omkeerbaar, het laatste niet. De onomkeerbaarheid van ingewikkelde biologische processen wordt vaak uitgedrukt – in relatie met de beruchte tweede wet van de thermodynamica – in zulke metaforen als ‘dat niemand in staat is om de gang van zaken terug te draaien’, zodat omgevallen bomen weer overeind komen, zichtbaar licht gaan uitstralen en kooldioxide afgeven, terwijl ze zuurstof opnemen, enzovoort.
Duncan Brown gebruikte in zijn colleges het voorbeeld van wat hij de ‘omgekeerde muisproef’ noemde. Eenieder snapt dat het onmogelijk is om muizenkeutels in de muizendarm te schuiven, warmte toe te voegen aan het muizenlijfje, kooldioxide in zijn longen te pompen, en dan te verwachten dat de muis zuurstof uitademt en de kaas uitspuugt die de bron van keutels vormde.
Het kan natuurlijk evengoed misleidend zijn om teveel nadruk te leggen op de constantheid. Het systeem is immer in een staat van verandering. Maar gedurende de eerste ontwikkelingsstadia worden de richting en het tempo van de verandering overheerst door de processen van successie. En in een rijp ecosysteem slingert de biomassa, de kwantitatieve soortensamenstelling, de totale metabolische activiteit, enzovoort soms tamelijk regelmatig wat heen en weer, maar het kan soms ook best chaotisch zijn. Dat kan voortkomen uit intrinsieke oorzaken, of het kan liggen aan seizoensfluctuaties, klimaatschommelingen en veranderingen in de topografie. Niettemin is een rijp systeem, zelfs met die variaties, stabieler en heel wat veerkrachtiger dan een systeem in het beginstadium van successie.
Lees in dit verband ook het artikel ‘Het principe van maximaal vermogen in de evolutie, ecologie en economie’ van Charles Hall en Timothy McWhirter in de rubriek Ecologie.

De groei van een levend organisme of een biologische gemeenschap is niet eenvoudig een kwestie van het produceren van meer levend weefsel uit het beschikbare voedselaanbod. Het is in feite een uitdrukking van het verschil tussen ‘anabolische’ of biosynthetische reacties enerzijds, en ‘catabolische’ of ontbindende reacties anderzijds. De anabolische reacties beslaan al die processen die de moleculen produceren waaruit levend weefsel wordt opgebouwd – vetten, eiwitten, polysachariden, nucleïnezuren, enzovoort. De catabolische reacties bestaan voornamelijk uit het afbreken van voedsel en reserve-‘brandstoffen’, zeker in heterotrofen, om te voorzien in zowel de energie als de grondstoffen die nodig zijn voor de anabolische processen, maar, daar bovenop, omvatten ze ook de ontbinding van bestaande, levende weefsels. Met andere woorden: vitale weefsels van een organisme worden voortdurend afgebroken en vernieuwd – ze worden, om het in economische termen te zeggen, voortdurend ‘omgezet’. Op het eerste gezicht mag dit een nogal zinloze exercitie lijken, maar het omvat, onder andere, potentiële reparatiemechanismen voor het organisme.
Binnen een soortengemeenschap is het samenstel van deze twee sets van processen misschien nog wel belangrijker, want hier wordt de collectieve ‘omzet’ niet alleen bepaald door de optelsom van de omzet van alle individuen, maar ook door de manier waarop de leden van de gemeenschap met elkaar in wisselwerking zijn.* Een dichte opeenhoping van planten zal hun biosynthetische reacties vertragen. Het gegeten worden van een plant of een dier zal de verwerking ervan op gang brengen en dit feestmaal zal de biosynthetische reacties van de consument juist stimuleren. Dit alles leidt tot een gemeenschappelijke ‘omzet’ van voedingsstoffen binnen een ecosysteem, waarover verderop meer. Het brengt ook een collectief energiemetabolisme voort dat in cijfers kan worden uitgedrukt, soms zeer precies, maar vaker bij benadering.
Het energiemetabolisme van een heterogene gemeenschap wordt weerspiegeld in de uitruil van kookdioxide en zuurstof met de atmosfeer. Het dierlijk leven boven de grond consumeert zuurstof en produceert kooldioxide, net als sommige bodemdieren en -planten. Dit is de netto uitdrukking van de ademhaling. De rest van het bodemleven, de anaeroben, geven kooldioxide af zonder zuurstof te consumeren. Sommige geven ook methaan af. De planten fotosynthetiseren overdag, met als netto resultaat dat er zuurstof geproduceerd wordt en kooldioxide opgenomen. ’s Nachts ademen de planten alleen uit met het omgekeerde resultaat.
De kwantitatieve verhouding tussen deze twee processen, fotosynthese en uitademing, bepaalt niet slechts de samenstelling van de atmosfeer op de lange termijn, maar is direct ook een bruikbare indicator voor wat er ergens aan de hand is. De netto mate waarmee de twee gassen, zuurstof en kooldioxide, worden uitgewisseld kun je omzetten in de mate van bruto fotosynthese (F) en de mate van bruto ademhaling (A).
In de vroege stadia van de kolonisatie van een bodem die nog niet goed bewoond is door heterotrofen, is F groter dan A omdat de planten pioniers zijn en ze dus groeien. Als het systeem rijper wordt en de totale biomassa toeneemt, vertraagt de groei van de biomassa echter verhoudingsgewijs, neemt de fotosynthese wat af en maakt de ademhaling een inhaalslag, zodat ten slotte in de theoretisch ideale situatie F gelijk is aan A. Dus is het quotiënt F/A = 1. Met andere woorden: er is geen netto toename in de zuurstofafgifte of kooldioxide-opname meer. F/A blijft natuurlijk alleen precies 1 in de menselijke verbeelding, al is het tropisch regenwoud er vermoedelijk nooit ver van af. In andere milieus zal het quotiënt veranderen met de omstandigheden. Het zal in gematigde wouden op- en neergaan met de seizoenen. In alle ecosystemen zal het fluctueren vanwege intrinsieke oorzaken. En in ecosystemen die om de een of andere reden in verval zijn, zal het quotiënt onder de 1 zakken.
Het doel van de landbouw is om het ecosysteem terug te dringen naar een vroeg stadium van successie, waarin het F/A-quotiënt hoog is. Daarover gaat het tweede artikel. Hier volgen eerst nog een paar belangrijke aanvullingen op het voorgaande.

Stoffen in de toplaag van een steriele planeet zullen van de ene naar de andere plek bewegen door seismische activiteit. Als de planeet een atmosfeer heeft kan de verplaatsing ook komen door winderosie. Als er enig vocht is, kan dat ook erosie met zich meebrengen. En als er genoeg vocht is, kan het geërodeerde materiaal zich in poeltjes verzamelen. De aanwezigheid van levende organismen verandert die toestand echter diepgaand en het bewegen van oppervlaktemateriaal wordt dan een zeer complex biologisch verschijnsel. Het leven in zijn geheel introduceert in het hele proces zo’n breed scala van biochemische transformaties dat we nu beter van het voortbewegen van voedingselementen kunnen spreken dan de term stoffen te gebruiken. En dat al helemaal omdat, zoals we hiervoor zagen, die elementen rondgaan in plaats van zomaar te bewegen en dat die kringloop afhankelijk is van de stroom zonnestraling.
Ecologieboeken bespreken biogeochemische kringlopen gewoonlijk per individueel chemisch element, zoals de koolstof/zuurstof/waterstofkringloop, de stikstofkringloop, de fosforkringloop, enzovoort. Dit is nogal gekunsteld, maar je ontkomt er bijna niet aan als je dit thema in detail wilt bekijken. Het is ook de gewoonte de kringlopen weer te geven in een plaatje met pijlen tussen de bij elkaar horende onderdelen, zodat je hokjes krijgt met ‘planten’, ‘dieren’, ‘bodemleven’, ‘anorganische afzettingen’, ‘oceanen’ en dergelijke. Daar probeert men dan vaak getallen bij te zetten om het relatieve belang weer te geven. Er kunnen ook getallen staan bij pijlen in de figuur. Zo zou je ook de vakjes in de figuur van het ecosysteem uit aflevering 2 kunnen interpreteren, als je daar behoefte aan hebt.
Elk element dat door een plant, dier of micro-organisme wordt opgenomen, wordt ook weer op de een of andere manier gerecycled. Dit geldt voor de elementen die de voornaamste bouwstenen van biologische moleculen zijn (zie verderop), voor algemeen voorkomende mineralen (zoals calcium, magnesium, natrium, kalium, ijzer, enzovoort), voor sporenelementen (zoals koper, molybdeen, kobalt, selenium, jodium, enzovoort) en voor onvoorziene, vreemde elementen. Het geldt voor elementen die snel rondgaan en voor de elementen die, voor de korte termijn, uit een kringloop lijken te verdwijnen en in relatief ontoegankelijke afzettingen worden geparkeerd, maar die niettemin over een zeer lange tijd gezien toch wel in de kringloop blijven.
Alle voedingselementen delen een of andere algemene transmissieroute. Die routes behelzen de directe inname van één organisme door een ander, het achterlaten van uitwerpselen en het daarop volgende incorpereren van de elementen die daar in zitten door andere organismen, de afbraak van dood plantaardig materiaal en de kadavers van dieren door (voornamelijk) bodemleven en ten slotte de opname van de elementen door hogere planten. De belangrijkste deelnemers aan de afbraak van afval verschillen per habitattype. Ze gaan van ongewervelde dieren met een zacht lichaam, zoals wormen, naaktslakken en huisjesslakken, die je vindt waar het lekker vochtig is, tot mieren en termieten, die in droge omgevingen de verantwoordelijkheid torsen.
Hier bovenop zijn er bijzondere reacties en kringloopmechanismen die specifiek horen bij die paar elementen die de belangrijkste onderdelen van de biologische moleculen uitmaken. Deze elementen zijn – in afnemende orde van de mate van hun voorkomen in de aardkorst – zuurstof, koolstof, stikstof, waterstof, fosfor en zwavel. Een essentieel onderdeel van de koolstof- en zuurstofkringloop is atmosferisch. De waterstofkringloop is nauw gekoppeld aan de kringlopen van koolstof en zuurstof, en, omdat enig water altijd wel in de vorm van waterdamp verkeert, is de kringloop van waterstof eveneens deels atmosferisch.
De langzame cycli van Gaia, die bij Earth Science horen, zijn net zo goed belangrijk om de werking van de natuur te begrijpen.

Stikstof hoeft niet atmosferisch rond te gaan omdat stikstofverbindingen direct kunnen worden opgenomen, of in opgeloste vorm doorgegeven; niettemin is een belangrijk deel van de stikstofkringloop atmosferisch. Dat komt door twee grote groepen bacteriën en door blauwalgen (ook wel cyanobacteriën genoemd). De groep van de denitrificerende bacteriën kan voor hun ademhaling toe met nitraat (NO3-) in plaats van zuurstof; ze produceren daarbij elementair (dus gasvormig) stikstof dat naar de atmosfeer ontsnapt. Als hun activiteiten niet door de groep van de stikstofbindende bacteriën en de blauwalgen gecompenseerd zouden worden, is het de vraag of er leven zou zijn op aarde. De stikstofbinders reduceren gasvormig stikstof in wezen tot ammoniak (NH3) dat wordt opgenomen in aminozuren en van daaruit in eiwitten en andere stikstofhoudende biologische moleculen.*
Ook zwavel hoeft niet via de atmosfeer rond te gaan, maar toch gebeurt dat met een deel. Met fosfor is het echter anders. Er zijn binnen de marges van de aan het aardoppervlak heersende temperaturen van nature weinig chemische vormen waarin fosfor vluchtig is; daarom is er geen atmosferische kringloop van enige betekenis. Precies dit gebrek aan vluchtige stofwisselingsproducten (metabolieten) maakt de fosforkringloop anders dan die van de andere vijf elementen waarover we het zonet gehad hebben. Daardoor heeft de landbouw van fosfor in wezen een niet-herbruikbare grondstof gemaakt.*
Een belangrijk kenmerk van elke reactievolgorde, of elk kringloopmechanisme, is de frequentie waarin het plaatsvindt. Omzettingsfrequenties in complexe systemen zijn moeilijk te meten, maar er zijn een paar nuttige indicatoren die ons tenminste in staat stellen vergelijkingen te maken tussen verschillende milieutypes. Eén zo’n indicator is het tempo waarin afval op de bodem van een bos terecht komt. Deze indicator is nuttig omdat de ontbinding van afval een belangrijke, soms overheersende bijdrage levert aan de ‘niet-plant-ademhaling’ van een ecosysteem. Er is voor vochtig tropisch regenwoud bijvoorbeeld gevonden dat het jaarlijks 1100 gram afval per vierkante meter produceert; vergelijk dat met zo’n 100 gram per vierkante meter in boreale bossen. Ga je van de evenaar naar de pool dan zie je de getallen bijna in een rechte lijn afnemen. A. Duncan Brown meent daarom te mogen stellen dat de omzetting van voedingsstoffen in tropische regenwouden ongeveer het tienvoudige is van bossen op hoge breedtegraden (of hoog op bergen gelegen bossen).*
Met de kringloopfrequentie van fosfor is het volgende aan de hand. Bodemfosfor kan op een aantal manieren ‘gebonden’ worden (namelijk als onoplosbare organische verbindingen, als organische verbindingen en vastgehecht aan geladen bodemdeeltjes), of het kan juist vrijelijk oplosbaar in water zijn, of in een verdunde natriumbicarbonaatoplossing. De oplosbare vormen zijn vrij beschikbaar voor planten, maar fosfor dat zo vast gebonden is dat het alleen kan worden losgemaakt met de kracht van vergisting met een zuur als heet waterstofperchloraat, of met de versmelting met soda (natriumcarbonaat), kun je normaal gesproken als ‘onbeschikbaar’ beschouwen.
Duncan Brown vindt dat in wezen alle fosfor beschikbaar is, maar dan in heel verschillende frequenties voor de oplosbare en vaste vormen. Gebonden fosfor is niet beschikbaar voor snelle groeiers, niet omdat het achter een ondoordringbare muur zit (want heel langzaam komt het toch vrij), maar omdat planten er niet snel genoeg bij kunnen om het stofwisselingsniveau te onderhouden dat ze nodig hebben om te groeien of in leven te blijven. Als planten echter intrinsiek in staat zijn om met een zeer langzame stofwisselingsfrequentie toe te kunnen, en als het ‘gebonden’ fosfor de enige beschikbare vorm is, dan zullen ze er gebruik van maken op grond van de verdienste van de langzame mobilisatie door microbiële activiteit en abiotische chemische veranderingen in de bodem. Er zijn flink wat plantensoorten die heel langzaam groeien doordat ze ingetoomd worden door zulke lage concentraties van het oplosbare fosfor. Ze komen daarom zeker niet in aanmerking als landbouwgewas.
Vanouds probeerden boeren de bodem voldoende vruchtbaar te houden door akkers braak te laten liggen, of met zwerflandbouw (in de tropen) steeds wat op te schuiven, om zo toch voldoende fosfor beschikbaar te maken.

Veel mensen menen dat dierlijke mest per saldo een toename van de bodemvruchtbaarheid oplevert, in plaats van dat het iets vervangt wat is weggehaald. Het onderscheid tussen deze twee interpretaties wordt natuurlijk bepaald door wat je onder ‘vruchtbaarheid’ verstaat. Als het het totale vermogen van de bodem tot een bepaalde oogstopbrengst inhoudt, of het in stand houden van een bepaalde biomassa, dan is het onderscheid terecht en het geloof in een grotere vruchtbaarheid gerechtvaardigd, omdat het opbrengen van dierlijke uitwerpselen kan bijdragen aan de bodemstructuur, het vasthouden van water, wormenpopulaties, enzovoort. Als je echter onder vruchtbaarheid de hoeveelheid voedingsstoffen in de bodem verstaat, dan vergt de bewering nadere kwalificatie.
Het omzetten van zaden, plantenweefsel of dierlijk weefsel in organische compost gaat sneller als dit gebeurt door de passage van het verteringskanaal van een dier dan in welk ander natuurlijk proces ook. Wat een dier in een dag voor elkaar krijgt, kost in een goed beheerd compostsysteem enkele weken, alhoewel de producten in meerdere opzichten van elkaar verschillen.
Een verteringskanaal is een compleet microbieel ecosysteem, dat van een ‘conventioneel’ (bij gebrek aan een betere term) aards systeem in principe alleen op het punt van de energiestroom verschilt. Een conventioneel systeem draait op een stroom stralingsenergie; een verteringssysteem wordt aangedreven met een stroom van chemische energie. In beide gevallen is de output ‘gedegradeerd’. De ongebruikte stralingsenergie wordt voornamelijk als hitte uitgestraald, terwijl de overbodige chemische energie uit het verteringssysteem wordt afgegeven als warmte en als afgebroken chemische verbindingen. In beide gevallen benadert het systeem een ‘steady state’, als je de reguliere schommelingen buiten beschouwing laat. In een verteringssysteem kun je schommelingen misschien beter omschrijven als ritmes, vooral bij roofdieren die grote maaltijden afwisselen met lange tussenpozen. Grazers benaderen de echte ‘steady state’ veel dichter – oftewel wat in een laboratorium of in de industrie bekend staat als een ‘permanente cultuur’.
Als het dier gewerveld is – en dat zijn dieren op de boerderij gewoonlijk – dan wordt het ruwe materiaal eerst vermalen met de tanden, of een beetje verderop, in een spiermaag. Vervolgens doorloopt het een perfect voor dit doel ontworpen demontagelijn, een soort omgekeerde lopende band. De voedingswaren komen langs een serie verteringsenzymen die werkzaam zijn als het watergehalte, de zuurgraad en de temperatuur precies goed zijn per type enzym. Als het dier een zoogdier of een vogel is – en ook dat zijn dieren op de boerderij gewoonlijk – is de temperatuur van rond de 37 graden Celsius niet alleen precies goed voor de werkzaamheid van de ter plekke aangemaakte verteringsenzymen, maar is het ook ideaal voor de groei en de stofwisseling van de massale populatie van de darmflora – voornamelijk bacteriën. Als het dier een pens heeft, is er ook nog een grote populatie protozoa (eencellige, vaak beweeglijke, heterotrofe eukaryoten zonder chloroplasten).
Het resultaat van de gecombineerde werking van de verteringsenzymen van het dier en die van de microbiële populatie is dat – binnen een dag voor grote dieren en veel sneller voor kleine – het residu van de twee processen van vertering en assimilatie als poep wordt uitgescheiden. Wat zit daarin? In een notendop (figuurlijk gesproken dan) bevat het wat de dieren aten minus wat ze er voor eigen gebruik aan hebben onttrokken. Duncan Brown richt zich dan even niet op wat het organisch inhoudt, maar op de voedingselementen zonder zich te bekommeren om hun scheikundige toestand. Een jong dier eet gedurende zijn groeiperiode om in zijn energiebehoefte te voorzien, en die haalt het uit de waterstof en koolstof in zijn voedsel, èn het eet om de voedingselementen te krijgen waaruit het nieuw weefsel en botten opbouwt en waarmee het ook het weefsel en de botten vervangt die worden afgebroken in het vernieuwingsproces dat we eerder al noemden. De uitwerpselen bevatten die elementen die niet zijn geassimileerd. De urine bevat die elementen welke in de weefselvervanging zijn vrijgekomen en alles wat als overbodig uit de ingewanden naar de bloedbaan is overgeheveld en verder niet gebruikt is. Koolstof dat gebruikt wordt in de energie-uitwisseling wordt merendeels uitgeademd. Het bijbehorende water vindt zijn weg naar het ‘metabolische’ water, dat, in geval van veel insecten, voldoende kan zijn om in de hele waterbehoefte te voorzien.
Ik vat nu het vervolg van het verhaal van Duncan Brown in een laatste aflevering samen, in plaats van het letterlijk te vertalen.

Dieren die vrij in de weide rondlopen, zullen de stoffen die ze door middel van het gras aan de bodem onttrekken daar ook weer uitpoepen. Dat kan gespreid gaan, maar meestal vindt concentratie plaats, bijvoorbeeld bij schapen die voor de nacht bijeengedreven worden, bij dieren die op stal staan, of waar de mest van de weide (of de heide) naar de akker wordt overgebracht.
Belangrijk is te beseffen dat een volgroeid dier met een constant gewicht in zijn poep en pies evenveel voedingselementen zal uitscheiden als het eet. Niet meer en niet minder, welke diersoort het ook is. Bij een efficiënte verteerder, zoals bij een herkauwer, zal een hoger aandeel van de verteerde elementen met de urine worden geloosd en een lager aandeel met de poep dan bij een ondoelmatige herbivoor. Maar in beide gevallen is het totaal (in poep en pies samen) gelijk aan wat er opgegeten werd.
Daaruit zou je de opmerkelijke conclusie kunnen trekken dat er geen limiet is aan hoeveel vee je in de wei toelaat. Maar dan vergeet je een paar andere factoren. Nog even afgezien van de bodemverdichting door zoveel hoeven, houd je dan geen rekening met de vele processen die de groeisnelheid van het gras en de ontbinding van de poep bepalen. En die worden mede bepaald door de seizoenen, de beschikbaarheid van water, de temperatuur en natuurlijk door het aantal grazende dieren. Dus als het tempo waarin per oppervlak gras wordt gegeten de groei van nieuw gras niet overtreft, zou je – op dit punt – het systeem duurzaam kunnen noemen. Het blijft wel belangrijk over welke tijdsduur je het bekijkt: tien jaar lang met daaronder één droog jaar geeft een ander antwoord dan een natte zomerperiode van zes maanden.
Maar blijven de voedingsstoffen die in de uitwerpselen zitten wel ter plaatse? Als ze oplosbaar zijn, en dat is in elk geval de toestand bij urine, kunnen ze uitspoelen, zodat ze niet meer beschikbaar zijn voor de planten. In de poep van herbivoren zitten de stoffen die planten nodig hebben niet in pasklare vorm. Dat komt omdat cellulose zo’n bijzonder weerbarstige substantie is. De vertering in de maag van de herbivoor is een anaeroob proces; er komt geen zuurstof aan te pas. Het is een serie fermentaties met een eindproduct waarin de voedingsstoffen nog zodanig chemisch gebonden zijn, dat de plant er niet bij kan. Eenmaal op de grond worden de uitwerpselen blootgesteld aan zuurstof, dat met behulp van de mechanische behandeling door ongewervelden en de biochemische behandeling door de bodemmicroflora, de afbraak een stuk verder brengt. De uitwerpselen worden gegeten en weer verspreid door dezelfde ongewervelden (vliegen, kevers, enzovoort) en veelal ook door gewervelden. Hoewel deze tweede fase van consumptie en vertering door dieren ook anaeroob is, helpt het toch aanzienlijk. Het komt er op neer dat de poep verspreid wordt en, misschien belangrijker, dat de verbindingen verder worden opgebroken waarbij voedingselementen vrijkomen die de planten kunnen opnemen.
Een kringloop van dierlijke uitwerpselen voegt dus per saldo niets toe aan de voedingselementen in de bodem, zegt Duncan Brown. De uitwerpselen kunnen op verschillende manieren de bodemkwaliteit bevorderen; maar die bevorderende processen zouden toch al hebben plaatsgevonden door de activiteiten van het bodemleven.
En er treedt door menselijk ingrijpen sowieso verlies op. Nemen we in dat verband fosfaat nog even onder de loep, dan zien we dat dieren die opgroeien het element vastleggen in hun lichaam. Bij een stier die opgroeit tot een gewicht van 700 kilogram, is dat 7 kilogram fosfaat. Die wordt dus onttrokken aan de bodem, definitief als de stier naar het slachthuis gaat en er niets van zijn lijf op het land terugkomt. Die 7 kilo fosfaat in de grond vervangen kost overigens 78 kilo superfosfaat (de mest waarvan de fosfaat ergens ter wereld gedolven moet worden – er is immers geen mondiale kringloop van enige betekenis). De Nederlandse veehouderij is intussen natuurlijk ver afgedwaald van het eenvoudige (kringloop)model.
Laten we, voordat we in het tweede artikel het gedrag van de boer onder de loep nemen, nog het bodemleven bekijken, eerst alleen de fascinerende schimmels en daarna het even fascinerende geheel.
Er worden bij het bodemleven aan de lopende band ontdekkingen gedaan. Omdat we het niet kunnen zien, hechten we er weinig waarde aan. Zo werken we het tegen in plaats van ermee samen te werken.

Het grootste organisme op aarde is níet de blauwe vinvis. Het heeft geen ogen en geen reukorgaan, maar evenmin bladeren of bloemen. Het is zelfs niet te zien als je er bovenop staat. Het is een schimmel met de naam Armillaria die leeft in de Blue Mountains in de Amerikaanse staat Oregon. Daar, over een oppervlak van zo’n tien vierkante kilometer, verspreiden de schimmeldraden zich langzaam door de bosbodem – hun snelheid wordt geschat op pakweg één meter per jaar. Samen vormen de witte, ragfijne draden een netwerk dat zwamvlok heet, of met een wetenschappelijker woord: mycelium. Het is een netwerk dat op z’n minst al tweeduizend jaar oud is.
Dat mysterieuze mycelium speelt een hoofdrol in het boek Verweven leven van de Britse mycoloog Merlin Sheldrake.* Hij beschrijft het als ‘een anarchistisch filigrein van tere, piepkleine buisjes’, als ‘ecologisch bindweefsel, de levende naad waarlangs de wereld voor een groot deel aan elkaar is genaaid’, als ‘een levensvorm die ons dierlijke voorstellingsvermogen op de proef stelt’. En mycelium is niet alleen aanwezig in de Blue Mountains, maar in elke bosbodem, in je achtertuin en soms zelfs in je huis.
Om mycelium beter te begrijpen is eerst wat schimmelkennis nodig. ‘Wereldwijd zijn er naar schatting ruim twee miljoen schimmels’, zegt Sheldrake aan de telefoon in een interview met de NRC.* Het interview werd afgenomen door Gemma Venhuizen en verscheen op 20 november 2020 in de krant. Ik citeer hier weer veel letterlijk (met dank aan de onvolprezen Gemma Venhuizen).
Een paar duizend van die schimmels zijn eencellig – dat zijn de gisten, die bijvoorbeeld voor brood en bier gebruikt worden – maar verreweg het grootste deel is meercellig en vormt een mycelium. ‘Ook die rottende sinaasappel op je fruitschaal. Dat witte, pluizige wat je ziet zijn de schimmeldraden, en soms zie je zelfs kleine paarsige puntjes: de sporen.’ Daarmee planten schimmels zich voort: uit elke spore groeien hyfen (dat zijn de afzonderlijke schimmeldraden) en die kunnen samen een compleet nieuw mycelium vormen.
Lang niet altijd groeien de sporen direct uit het mycelium. Soms verspreiden ze zich via vruchtlichamen: de paddenstoelen. Zo is het coniferenbos in de Blue Mountains bezaaid met honingzwammen – samen vormen ze het kleine stukje van de gigantische Armillaria dat níét aan het oog onttrokken is. Sheldrake: ‘Vergelijk het met een appelboom waarvan je alleen de appels zou zien.’ Er bestaan zo’n 20.000 verschillende soorten paddenstoelen. Bij sommige soorten komt er een grote sporenwolk vrij als je erop gaat staan (zoals bij de stuifzwammen), bij andere soorten zitten de sporen tussen lamellen of in buisjes onder de hoed (de plaatjes- en buisjeszwammen). En dan zijn er nog de truffels: ondergrondse paddenstoelen, die sterk geuren zodat ze door dieren worden opgegraven en op die manier hun sporen kunnen verspreiden. ‘Wanneer we het aroma van een truffel ruiken, ontvangen we een boodschap van de truffel aan de wereld’, staat in Verweven leven.
Het zijn niet alleen de paddenstoelen en hun sporen die bijdragen aan de myceliumvorming. Ook de hyfen spelen daarin een actieve rol. Die kunnen zich vertakken en verbindingen aangaan met andere hyfen. Ze moeten in staat zijn om elkaar te herkennen, zegt Sheldrake, zodat ze weten of ze met een mogelijk vijandige soort te maken hebben, óf met een mogelijke voortplantingspartner. Want ook hyfen hebben seks. Of zoals Sheldrake het uitlegt in zijn boek: ‘Wil een zwartetruffelzwam bijvoorbeeld vrucht dragen, dan moeten de hyfen van het ene myceliumnetwerk zich verenigen met die van een ander afzonderlijk, geslachtelijk compatibel netwerk en er genenmateriaal mee delen.’
Truffelzwammen zijn onder te verdelen in twee ‘paringssystemen’, voegt hij toe: plus en min. ‘Van voortplanting is sprake wanneer een min-hyfe een plus-hyfe aantrekt en ermee versmelt. De ene partner heeft een vaderrol en levert uitsluitend genenmateriaal. De andere speelt een moederrol, want levert genenmateriaal én voorziet in het ‘vlees’ dat rijpt tot truffels en sporen.’
Hierna het vervolg van dit interview, met daarna nog een aflevering over schimmels met Toby Kiers als bron.

Hyfen gaan niet alleen met elkaar verbindingen aan, maar ook met andere levensvormen, vertelt Sheldrake enthousiast. Met algen bijvoorbeeld (‘een korstmos is een gearrangeerd huwelijk tussen schimmels en algen’), maar ook met de uitlopers van boomwortels. In dat laatste geval ontstaan er mycorrhiza: samenwerkingsverbanden tussen schimmeldraden en wortelstelsels. Het is een mutualistisch verbond: beide soorten profiteren ervan. Dit in tegenstelling tot bijvoorbeeld parasitaire schimmels of saprofyten (die voedingsstoffen onttrekken aan dode organismen). De samenwerkende schimmels krijgen koolstof aangeleverd vanuit de boom, en de bomen krijgen voedingsstoffen als stikstof en fosfor die de schimmels aan de bodem onttrekken. ‘Voor de mens is die samenwerking interessant, want veel mycorrhizaschimmels produceren eetbare paddenstoelen’, zegt Sheldrake. ‘Truffels, eekhoorntjesbrood, cantharellen, matsutake… Maar voor de bomen is het schimmelnetwerk essentieel.’
Al ruim twintig jaar spreken biologen van het wood wide web als ze het hebben over die ondergrondse transportsystemen tussen bomen. In het boek Benedenwereld, uit 2019, beschrijft de Britse natuurschrijver Robert Macfarlane hoe hij met Sheldrake op excursie gaat en over het nut van dit wood wide web praat: ‘Het schimmelnetwerk stelt planten ook in staat om stoffen uit te wisselen, zoals suikers, stikstof en fosfor. Een boom die doodgaat kan zijn stoffen bijvoorbeeld aan het netwerk afstaan, zodat de gehele gemeenschap ervan profiteert, en een boom die het zwaar heeft kan worden ondersteund met voedingsstoffen van de bomen ernaast.’ Sheldrake zelf schrijft in zijn boek ook over rhizomorfen: holle bundels van hyfen. ‘Omdat afzonderlijke hyfen hol zijn en dus geen draden […] zijn rhizomorfen lange buizen die uit vele kleine buisjes bestaan. Ze kunnen vloeistof veel sneller transporteren dan een afzonderlijke hyfe – volgens één waarneming met bijna anderhalve meter per uur – en maken het myceliumnetwerken mogelijk om over grote afstanden voedingsstoffen en water te vervoeren.’ Als voorbeeld noemt hij een bos in Zweden waar een Armillaria-mycelium een rhizomorf vormde om een stroompje over te steken: de hyfenbundel hing in een kronkelende streng aan de onderkant van de brug.
En dat werpt de vraag op: hoe dóén die hyfen dat allemaal? Hoe ‘weten’ ze waar ze moeten zijn? ‘De meeste schimmels zijn heel gevoelig voor licht, vocht en temperatuur’, zegt Sheldrake. ‘En hyfen kunnen de textuur van oppervlakten voelen. Ze bevinden zich in een brij van zintuiglijke informatie en ze hebben als het ware een sensorisch datasysteem geïntegreerd om zich te oriënteren. Maar waar dieren hun hersenen gebruiken om keuzes te maken, hebben myceliumnetwerken geen uniek, centraal besturingssysteem.’
Hij vertelt over het werk van de Zweedse mycoloog Stefan Olsson, die micro-elektroden in de hyfen van een Armillaria-myceliumnetwerk stak, en zo ‘regelmatige, actiepotentiaalachtige impulsen’ waarnam, die met pakweg een halve millimeter per seconde door het schimmelnetwerk heengingen. ‘Olsson vermoedt dat schimmels met elektrische signalen berichten tussen verschillende delen van zichzelf kunnen verzenden: over voedsel, verwondingen en dergelijke.’ Hoe dat precies in zijn werk gaat is nog onduidelijk, maar vermoedelijk hangt het samen met het openen en sluiten van poriën in de hyfen, zegt Sheldrake. ‘Het klinkt sciencefictionachtig, maar je ziet het bijvoorbeeld ook bij planten, algen en bacteriën – er zijn bacteriën die lange nanodraden produceren, met vezels die elektriciteit geleiden.’
Hoewel een schimmelcomputer op basis van die signalen voorlopig nog toekomstmuziek is, zijn er al wetenschappers die biocomputers maken van slijmzwammen, schrijft Sheldrake. Die zouden gebruikt kunnen worden om de omgeving te monitoren. ‘Schimmels zouden veranderingen in de kwaliteit van de bodem of van water kunnen signaleren, net als verontreinigingen en andere aspecten van de omgeving waar ze gevoelig voor zijn.’
We kunnen schimmelnetwerken dus maar beter intact laten, onwetend als we zijn.

Toby Kiers, hoogleraar evolutie aan de Vrije Universiteit Amsterdam, is net als Merlin Sheldrake een myceliumpionier.* Zij is een cartograaf van de ondergrond. In 2021 richtte ze de wetenschappelijke organisatie SPUN op, voluit de Society for the Protection of Underground Networks, om het belang van mycorrhiza onder de aandacht te brengen én om de wereldwijde verspreiding van hun gemeenschappen in kaart te brengen.* Ook het interview met haar is weer van Gemma Venhuizen. Het verscheen in de NRC van 3 februari 2023 (wetenschapsbijlage) met de kop ‘Blik op het schimmelrijk’.*
Lang, schrijft Venhuizen, lag het mycelium buiten het blikveld van wetenschappers, net als de rest van het schimmelrijk. Tot eind jaren zestig werden schimmels door biologen zelfs gewoon nog bij de planten ingedeeld. Nog altijd is onbekend hoeveel soorten er zijn, en waar en in welke samenlevingsverbanden ze voorkomen, en dus probeert Kiers, als een hedendaagse ontdekkingsreiziger, de blanco plekken op de wereldkaart in te vullen. Van de voedselarme eilandatollen in de Stille Oceaan tot aan de Italiaanse Apennijnen, en van de uitgestrekte vlaktes in Patagonië tot aan de binnenlanden van Lesotho: overal waar onvoldoende informatie voorhanden is, neemt Kiers samen met lokale wetenschappers bodemmonsters.
Het opgraven van myceliumnetwerken is ‘precisiewerk’, voegt Kiers toe. ‘Om die reden doen we het in eerste instantie samen met lokale wetenschappers. Maar het doel is om uiteindelijk overal ‘myconauten’ op te leiden, myceliumexperts die de ondergrondse netwerken monitoren en de wereldkaart up-to-date houden met gegevens over schimmelbiodiversiteit en bodemgesteldheid. Met hulp van algoritmes en kunstmatige intelligentie proberen we de kaart nog gedetailleerder te maken, al laten we ook zien over welke plekken en parameters we nog te weinig gegevens hebben. Je te veel blindstaren op een kaart is gevaarlijk, omdat het altijd een benadering van de waarheid is.’
‘Na mijn promotie was ik werk van de Franse econoom Thomas Piketty gaan lezen, en het viel me op hoe schimmels handig inspelen op de behoefte van planten. Ze gaan actief op zoek naar de plant die de meeste voedingsstoffen nodig heeft – op die plek wordt hun eigen onderhandelingspositie sterker – en sluiten dan gunstige deals. In de regel geldt: hoe meer stikstof en fosfor ze aanleveren, des te meer koolstof ze terugkrijgen. ‘Om die reden is het stikstofoverschot ook problematisch voor de mycorrhizavormers. Want hoe rijker de omgeving is aan stikstof, des te minder planten afhankelijk zijn van schimmels.’
Door voedingsstoffen met verschillend gekleurde nanodeeltjes (‘quantum dots’) te markeren, konden Kiers en haar collega’s zien hoe het transport door de schimmelnetwerken in detail verloopt. De plaats van handeling, het epicentrum van de stock exchange, zijn de plantenwortels. Sommige mycorrhizaschimmelsoorten dringen de wortels daadwerkelijk binnen, andere soorten omklemmen ze alleen, maar in beide gevallen vindt er uitwisseling plaats van voedingsstoffen. Kiers: ‘Je kunt mychorrhizaschimmels vergelijken met coöperaties. Ze handelen niet individueel maar groepsgewijs.’
De genetica van schimmeldraden is uiterst complex, benadrukt ze. Sommige mycorrhiza kunnen zelfs twee verschillende typen celkernen hebben. Het lijkt erop dat een plant bij voorkeur onderhandelt met mycorrhiza die wél dezelfde genetische celkern hebben, oftewel: tot dezelfde co-op behoren. De mycorrhiza met afwijkende celkernen vormen dan een andere co-op, en onderhandelen met andere planten.
‘Juist die samenwerkingen vind ik fascinerend om te zien. En stel je voor, die interacties zijn al zo’n 450 miljoen jaar aan de gang. Toen hielpen vroege mycorrhizavormen de vroege planten vermoedelijk om zich op land te vestigen, door gesteenten af te breken en de voedingsstoffen aan de planten te voeden.’ Schimmels, wil ze maar zeggen, zijn geen frivole accessoires van planten – ze zijn essentieel voor hun overleving. ‘Ik vergelijk ze graag met levende algoritmes die ingewikkelde puzzels kunnen oplossen.’*
Langzaamaan wordt de technologie ontwikkeld om de ondergrond beter in kaart te brengen, zegt Kiers. ‘Denk aan 3D-scanners, microsensoren… Mijn hoop is dat we de ondergrond net zo intensief gaan onderzoeken als de ruimte.’*
Hoe kan je als tuinier het bodemleven voor je karretje spannen (in plaats van het te verstoren met kwalijke gevolgen voor je opbrengst)? Over die vraag zullen we ons nu buigen.

In het (nog door mij uitgegeven) boek Het bodemvoedselweb – alle kleine beestjes helpen (nu bij uitgeverij Vonk!), geschreven door Jeff Lowenfels & Wayne Lewis en vertaald door Marc Siepman, wordt de lezer toegesproken als tuinier. Maar de inleiding van het boek kan ook dienen als een uitstekende samenvatting van wat er gebeurt in dat deel van de natuur dat zich letterlijk aan ons blikveld onttrekt. Laten we dus kijken wat dit boek ons te vertellen heeft:
Wie tuiniert is er zich ongetwijfeld van bewust dat er in een goede bodem regenwormen zitten; en met een beetje geluk weet je ook van ander leven op of in de bodem, zoals: duizendpoten, springstaarten, mieren, naaktslakken, larven van het lieveheersbeestje en nog veel meer. Het meeste van dit leven zit op of in de bovenste 10 centimeter; maar er zijn ook bodemmicroben gevonden die comfortabel op een diepte van ruim drie kilometer leven. Een goede bodem bestaat echter niet uit zomaar een paar beestjes. Een goede bodem krioelt van het leven.
Naast alle bodembeestjes die je kunt zien (er zitten bijvoorbeeld wel 500 regenwormen onder een vierkante meter gezonde bodem), is er een hele wereld vol organismen die je niet kunt zien, tenzij je dure optische instrumenten gebruikt. Alleen dan worden de microscopisch kleine organismen – bacteriën, schimmels, protozoa, nematoden – zichtbaar, en in verbijsterende aantallen. Een theelepeltje goede tuingrond bevat, zo hebben microbe-genetici gemeten, een miljard onzichtbare bacteriën, meters schimmeldraden, enkele duizenden protozoa en een paar dozijn nematoden. (Protozoa zijn de amoeben, pantoffeldiertjes, zweephaardiertjes en trilhaardiertjes. Nematoden zijn niet-gesegmenteerde, blinde rondwormen.*)
Voor al het bodemleven geldt: het heeft energie nodig om te overleven. Hoewel enkele bacteriën, die bekend staan als chemosynthetiseerders, hun energie uit zwavel-, stikstof- of zelfs ijzerverbindingen halen, moet de rest zijn energie halen uit iets waar koolstof in zit om te blijven leven. Koolstof kan komen uit plantenresten, of uit de uitwerpselen of overblijfselen van andere organismen. Bovenaan het prioriteitenlijstje van al het bodemleven staat: ‘koolstof verkrijgen voor de stofwisseling’ – het is een wereld van eten en gegeten worden, zowel in de bodem als er bovenop.
Er bestaat in Amerika een liedje van een oude vrouw die per ongeluk een vlieg inslikte. Wat deed ze daaraan? Ze slikt vervolgens een spin in (‘die wriemelde en kriebelde binnenin’) om de vlieg te vangen, daarna een vogel om de spin te vangen, enzovoort, tot ze een paard eet en sterft (‘uiteraard!’). Als je een schema maakt van wie geacht wordt wie te eten, beginnend bij de vlieg en eindigend bij het onwaarschijnlijke paard, dan krijg je een voedselketen. Maar de meeste organismen eten natuurlijk meer dan één soort prooi, dus als je een schema maakt van wie in de bodem wie eet, wordt de rechtlijnige keten een reeks ketens die gekoppeld zijn en elkaar overlappen, met andere woorden: je krijgt een bodemvoedselweb.
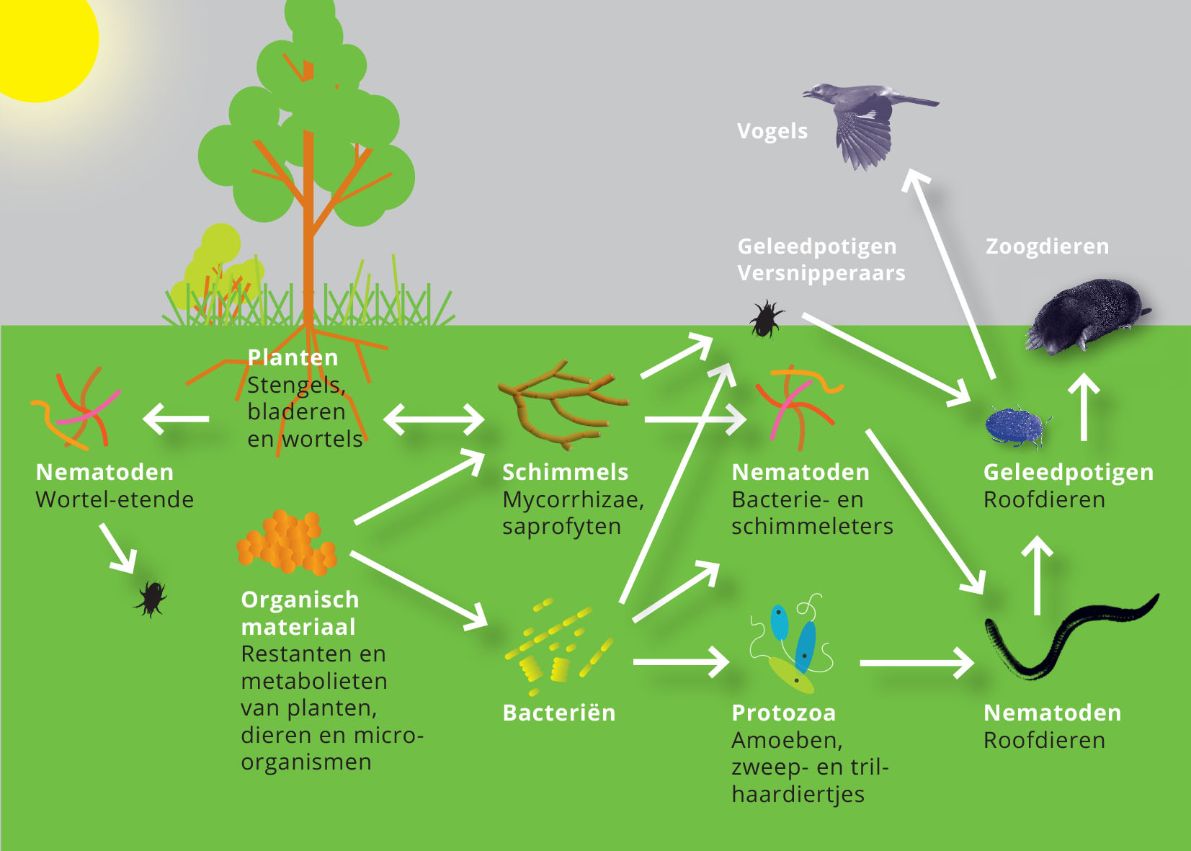
Figuur 5: Hier zie je een sterk vereenvoudigde weergave van een bodemvoedselweb. Maar zoals je je kunt voorstellen vertegenwoordigen deze en andere diagrammen complexe en zeer ontwikkelde reeksen van interacties, relaties en chemische en fysische processen. Het verhaal dat elke reeks vertelt is echter eenvoudig en begint altijd bij de plant.
Jeff Lowenfels heeft ook een heel goed boek over plantenfysiologie geschreven, getiteld Teaming with Nutrients :The Organic Gardener’s Guide to Optimizing Plant Nutrition (dat niet vertaald is).
De meeste tuiniers denken dat een plant alleen maar voedingsstoffen via het wortelstelsel opneemt en daarmee de bladeren voedt. Weinigen realiseren zich dat een plant 97 procent van zijn droge biomassa uit de lucht haalt door middel van fotosynthese. Een flink deel van de energie uit fotosynthese wordt gebruikt om chemische stoffen te produceren die de planten via de wortels uitscheiden. Deze uitscheidingen heten exudaten. Een goede analogie is zweet: het is een exudaat van mensen dat, net als bij planten, beschermende bacteriën aantrekt.
Exudaten komen uit de wortel in de vorm van koolhydraten (suikers) en eiwitten (proteïnen). De aanwezigheid van exudaten zorgt voor het aantrekken en voeden van specifieke nuttige bacteriën in de bodem, die leven van deze exudaten en van de afgestorven plantencellen die bij de groei van de wortel vrijkomen. Dit vindt allemaal plaats in de rhizosfeer, een zone die zich ongeveer twee millimeter rond de wortels bevindt. De rhizosfeer, die er onder de elektronenmicroscoop uit kan zien als jam of drilpudding, bevat een constant wisselende mix van bodemorganismen, waaronder bacteriën, schimmels, nematoden, protozoa en zelfs grotere organismen. Al dit ‘leven’ wedijvert om de exudaten in de rhizosfeer, of het water en de mineralen die erin zitten.
Onderaan in het bodemvoedselweb bevinden zich de bacteriën en de schimmels, die worden aangetrokken door de wortelexudaten en deze opeten. Op hun beurt worden zij weer gegeten door grotere microben, met name nematoden en protozoa, die ze voornamelijk voor de koolstof eten zodat hun stofwisseling kan blijven draaien. Alles wat ze niet nodig hebben wordt als afval weer uitgescheiden in een vorm die planten rechtstreeks kunnen opnemen. Het is handig dat de productie van voedingsstoffen in de rhizosfeer plaatsvindt, precies waar de plant ze kan opnemen.
Centraal in elk levensvatbaar voedselweb staan de planten. Planten hebben de controle over het bodemvoedselweb en doen daar hun voordeel mee, een verbazingwekkend feit dat door weinigen wordt begrepen en door tuiniers die ingrijpen in het systeem van de natuur zeker niet op waarde wordt geschat. Onderzoeken wijzen uit dat planten, door de exudaten die ze produceren, invloed uitoefenen op de aantallen en soorten schimmels en bacteriën die worden aangetrokken tot de rhizosfeer. En aangezien verschillende soorten organismen verschillende soorten voedingsstoffen mineraliseren, kunnen planten dus bepalen welke voedingsstoffen er in de rhizosfeer beschikbaar komen. Gedurende het groeiseizoen nemen de populaties van de schimmels en bacteriën toe en weer af, afhankelijk van de hoeveelheid voedingsstoffen die de plant nodig heeft en welke exudaten hij produceert.
Bodembacteriën en schimmels lijken op kleine zakjes mest, want ze bevatten stikstof en andere voedingsstoffen die ze uit exudaten en ander organisch materiaal (zoals de afgestorven wortelpunten) hebben gehaald. Om deze analogie nog wat verder door te voeren: protozoa en nematoden dienen als ‘meststrooiers’, doordat ze de voedingsstoffen vrijmaken die opgeslagen zaten in de bacteriën en schimmels (de ‘mestzakjes’). De nematoden en protozoa komen dus langs in de rhizosfeer en eten de bacteriën en schimmels. Ze nemen op wat ze nodig hebben en de overtollige koolstof en andere voedingsstoffen scheiden ze uit als afval.
Als je ze hun gang laat gaan, dan produceren planten exudaten waarmee ze schimmels en bacteriën aantrekken (en indirect ook nematoden en protozoa); hun overleven hangt af van de interactie tussen deze microben. Het is een volledig natuurlijk systeem, hetzelfde dat planten heeft gevoed sinds hun ontstaan, tweeënhalf miljard jaar geleden. Het bodemleven levert de voedingsstoffen die nodig zijn voor de planten, terwijl planten de cyclus initiëren en hem in stand houden door exudaten uit te scheiden. (Maar je kunt het natuurlijk ook omdraaien: de planten zijn dienstplichtig aan het bodemleven. Het is maar hoe je het bekijkt.)
Jeff Lowenfels heeft bovendien een boek geschreven over de hulp van schimmels bij tuinieren, dat wel vertaald is: Mycorrhizale schimmels en hun toepassingen, verschenen bij uitgeverij Vonk!
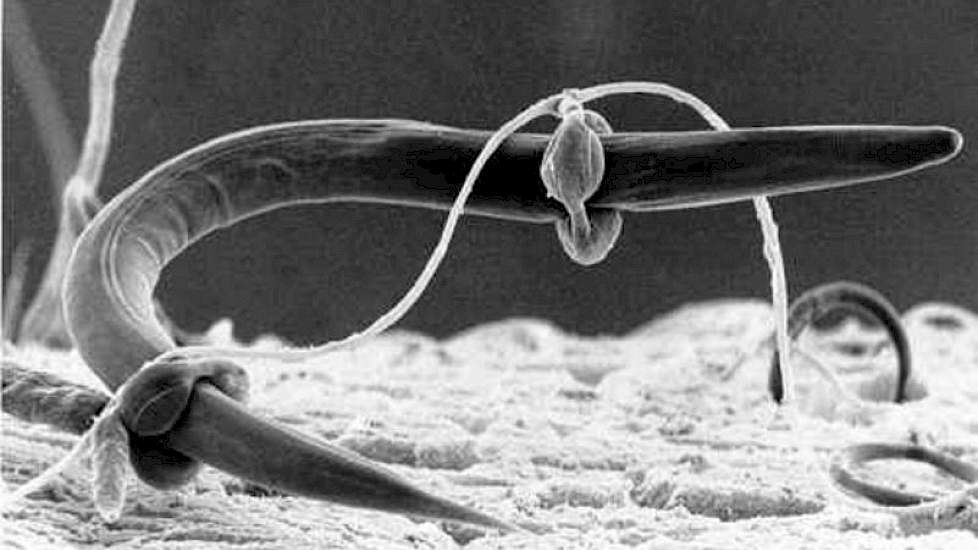
De protozoa en nematoden die de door exudaten aangetrokken schimmels en bacteriën opeten, worden op hun beurt opgegeten door geleedpotigen (dieren met gesegmenteerde lichamen, gelede poten en een harde buitenkant, het exoskelet). Insecten, spinnen en pissebedden zijn geleedpotigen. Geleedpotigen in de bodem eten elkaar en zelf zijn ze voedsel voor slangen, vogels, mollen en andere dieren. Je zou kunnen zeggen dat de bodem één groot fastfoodrestaurant is. Tijdens het zoeken naar eten bewegen de leden van een bodemvoedselweb zich door de bodem en beïnvloeden de structuur.
Bacteriën zijn zo klein dat ze zich ergens aan vast moeten plakken, anders spoelen ze weg. Dat doen ze door een slijmlaagje te produceren. Bijkomend effect is dat de bodemdeeltjes ook aan elkaar blijven plakken (net als bij tandplak, dat zijn mondbacteriën die zich in de loop van de nacht aan je tanden hechten). Schimmeldraden groeien ook tussen de bodemdeeltjes, hechten zich eraan en rijgen ze aan elkaar tot aggregaten.*
Wormen, samen met insectenlarven, mollen en andere gravende dieren, bewegen zich door de bodem op zoek naar voedsel en bescherming, en maken gangenstelsels waardoor lucht en water de bodem kunnen binnenkomen en weer verlaten. Zelfs microscopische schimmels helpen hierbij. Het bodemvoedselweb helpt dus, naast dat het voedingsstoffen in de rhizosfeer aflevert, ook om structuur aan de bodem te geven: de activiteiten van de leden binden bodemdeeltjes aan elkaar en tegelijkertijd verbeteren ze de doordringbaarheid voor water en lucht.
Als een lid van een bodemvoedselweb sterft, dan wordt het voer voor andere leden van de gemeenschap en zo worden de voedingsstoffen die opgeslagen zitten in het lichaam van een organisme doorgegeven. Een groter roofdier eet zo’n organisme misschien levend, of anders vergaan ze nadat ze dood zijn gegaan. Hoe dan ook zijn schimmels en bacteriën betrokken in het afbreken van het organisme, of in het afbreken van de mest van de succesvolle eter. Het maakt niet uit. Voedingsstoffen blijven behouden en worden uiteindelijk opgeslagen in de lichamen van zelfs de kleinste schimmels en bacteriën. Als deze organismen zich in de rhizosfeer bevinden, dan komen de voedingsstoffen in plantopneembare vorm vrij zodra zij weer opgegeten worden of doodgaan.
Zonder dit systeem zouden de meeste belangrijke voedingsstoffen uit de bodem spoelen. Nu blijven ze behouden in de lichamen van het bodemleven. Als je als tuinier of boer chemische meststoffen gebruikt, komt een klein deel ervan in de rhizosfeer, waar het opgenomen wordt, maar het grootste gedeelte verdwijnt uiteindelijk in het grondwater. Voor organisch gebonden voedingsstoffen geldt dit niet, die zijn wat men noemt geïmmobiliseerd. Deze voedingsstoffen worden uiteindelijk als afval weer uitgescheiden, dit heet mineralisatie. Als de planten zelf sterven en ontbonden worden, dan worden de voedingsstoffen die zij bevatten opnieuw geïmmobiliseerd in de schimmels en bacteriën waar ze door verteerd worden.
De aanvoer van voedingsstoffen in de bodem wordt nog op andere manieren door het bodemleven beïnvloed. Wormen trekken bijvoorbeeld organisch materiaal de bodem in, alwaar het versnipperd wordt door pissebedden en insecten (en hun larven), zodat schimmels en bacteriën ze verder kunnen verteren. Deze wormenactiviteit levert zo nog meer voedingsstoffen op voor de bodemgemeenschap.
In het schema van Lindeman (aflevering 72 van artikel 3 van ‘Wat is ecologie?’) staan de hier besproken soorten als ‘afbrekers’ in één hokje bij elkaar. Maar feitelijk vormen ze een systeem op zich en worden ze daar tekort gedaan.
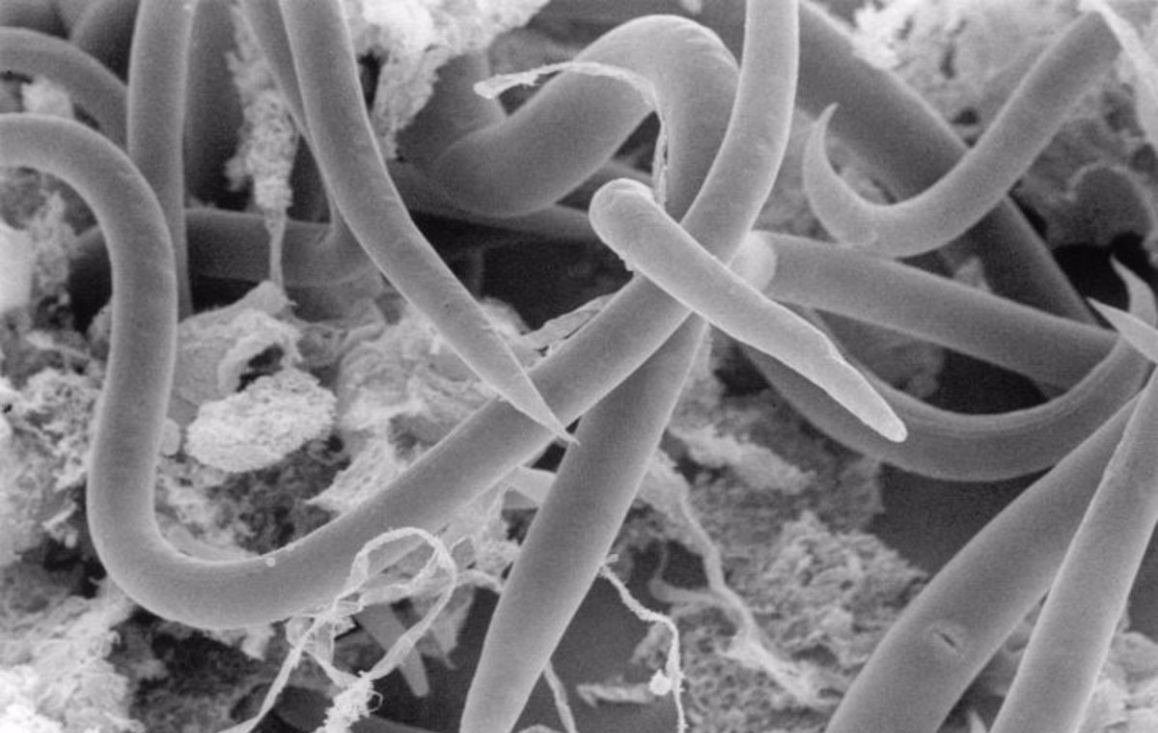
Een gezond bodemvoedselweb is er een dat niet verstoord wordt door ziekteverwekkende organismen. Tenslotte zijn niet alle bodemorganismen heilzaam. Als tuinier weet je dat ziekteverwekkende bacteriën en schimmels velerlei plantenziekten veroorzaken. Een gezond bodemvoedselweb bevat niet alleen enorme hoeveelheden individuele organismen, maar ook een grote diversiteit. Herinner je je dat theelepeltje met gezonde grond? Die miljard bacteriën bestaan uit misschien wel 20.000 tot 30.000 verschillende soorten – een gezonde populatie in aantallen èn in diversiteit.
Een grote en diverse gemeenschap houdt de lastposten (pathogenen) in bedwang. Een goede analogie is een dief op een drukke markt: als er genoeg mensen van allerlei slag zijn, dan zullen ze de dief vangen of zelfs voorkomen dat hij wat steelt (en het is in hun eigen belang dat te doen). Als de markt echter half verlaten is, dan zal de dief zijn gang kunnen gaan, net als wanneer hij sterker, sneller of op een andere manier beter is aangepast dan zijn achtervolgers.
In de wereld van het bodemvoedselweb vangen de nuttige organismen meestal geen dieven (hoewel het wel gebeurt: er zijn schimmels die nematoden te grazen nemen, zoals op de foto); het is meer dat ze met elkaar concurreren om exudaten of andere voedingsstoffen, lucht, water en zelfs ruimte. Als het bodemvoedselweb gezond is, dan zal dat de pathogenen in toom houden; ze kunnen zelfs doodgeconcurreerd worden.
Net zo belangrijk is dat elk lid van het bodemvoedselweb een plaats heeft in de bodemgemeenschap. Allemaal, op het oppervlak en daaronder, spelen ze een specifieke rol. Eliminatie van slechts één groep kan zo’n gemeenschap drastisch veranderen. Zo spelen vogels een rol door protozoa mee te laten liften op hun poten, of door een worm uit het ene gebied te laten vallen in het andere. Maar als er te veel katten komen verdwijnen de vogels en gebeurt dat niet meer. Mest van zoogdieren biedt voeding voor kevers in de bodem. Als je de zoogdieren doodt, of je vernietigt hun leefgebied of voedselbron (wat op hetzelfde neerkomt), dan heb je een stuk minder kevers. Andersom geldt hetzelfde. Een gezond bodemvoedselweb zal voorkomen dat één soort organismen zo sterk wordt dat ze het web vernietigen. Als er te veel nematoden en protozoa zijn, dan komen de bacteriën en schimmels die ze eten in de problemen en uiteindelijk ook de planten in hun omgeving.
Er zijn nog vele andere voordelen. De netten of webben die schimmels vormen rond wortels functioneren als fysieke barrières tegen invasies en beschermen planten tegen pathogene schimmels en bacteriën. Bacteriën bevolken oppervlakken zo doeltreffend, dat er geen plek meer is voor anderen om zich te hechten. Als iets deze schimmels of bacteriën aantast waardoor hun aantallen afnemen, dan kan de plant gemakkelijk aangevallen worden.
Speciale bodemschimmels, de mycorrhizale schimmels – we zagen het in de afleveringen 30-32 – vestigen zich in een symbiose met plantenwortels, waardoor die niet alleen een fysieke bescherming krijgen, maar ook nog voedingsstoffen aangeleverd krijgen. In ruil voor exudaten leveren deze schimmels water, fosfor en andere voor planten belangrijke voedingsstoffen. De populaties in het bodemvoedselweb dienen (vanuit het perspectief van de tuinder) in balans te zijn, anders worden deze schimmels opgegeten en dat gaat ten koste van de plant.
Bacteriën produceren zelf ook exudaten, en het slijm waarmee ze zich aan oppervlakken hechten vangt ook pathogenen. Soms werken bacteriën samen met schimmels in het vormen van beschermende lagen, niet alleen in de rhizosfeer, maar in een vergelijkbaar gebied rond de bladeren, de fyllosfeer. Bladeren produceren exudaten die micro-organismen aantrekken op exact dezelfde wijze als wortels dat doen; die organismen werken als barrière tegen invasies van ziekteverwekkende organismen.
Sommige schimmels en bacteriën produceren remmende stoffen, zoals vitaminen en antibiotica, die de plant gezond houden of maken; penicilline en streptomycine worden bijvoorbeeld respectievelijk door een bodemschimmel en een bodembacterie geproduceerd.
Owen zet de hier besproken soorten enigszins gemakkelijk weg als dienstverleners in de natuur, terwijl in de afleveringen van dit artikel over successie pathogenen ongenoemd blijven. Zie ook aflevering 69 en 70 van artikel 3 van ‘Wat is ecologie?’. En lees de vergelijking tussen biomassa en bbp die aflevering 71 maakt.

Uiteindelijk, vanuit de optiek van de plant in ieder geval, is het doel van het bodemvoedselweb om voedingsstoffen af te breken tot ze tijdelijk geïmmobiliseerd zijn in de lichamen van bacteriën en schimmels om daarna gemineraliseerd te worden. Naast koolstof is stikstof de belangrijkste van deze voedingsstoffen – het is de belangrijkste bouwsteen van aminozuren en daardoor van het leven. De biomassa van schimmels en bacteriën (de totale hoeveelheid van beide dus) bepaalt grotendeels de hoeveelheid stikstof die direct beschikbaar is voor gebruik door planten.
Pas sinds de jaren 80 van de vorige eeuw kunnen bodemwetenschappers de hoeveelheden bacteriën en schimmels precies meten. Dr. Elaine Ingham, van de Oregon State University (OSU) heeft samen met anderen een onderzoek gepubliceerd dat de verhouding van deze organismen in verschillende bodemtypen liet zien. In het algemeen kun je stellen dat de minst verstoorde bodems (die onder oerbossen) veel meer schimmels hadden dan bacteriën, terwijl verstoorde bodems (geploegde bodems bijvoorbeeld) veel meer bacteriën hadden dan schimmels. Deze en latere studies laten zien dat landbouwbodems een schimmel-bacterieverhouding hebben van 1:1 of minder, terwijl bosbodems minstens tien keer zo veel schimmels hebben als bacteriën. Ingham en een aantal van haar studenten van de OSU merkten ook een verband op tussen planten en hun voorkeur voor bodems die door schimmels of door bacteriën gedomineerd werden, of die neutraal waren. Aangezien de weg die een bodem aflegt van bacterie- naar schimmeldominant ongeveer dezelfde is als bij natuurlijke successie, werd het makkelijk om te voorspellen wat voor soort bodem een plant het liefst zou hebben door te kijken naar waar hij vandaan kwam. In het algemeen hebben meerjarigen – bomen en struiken – de voorkeur voor schimmeldominante bodems, terwijl eenjarigen en groenten bacteriedominante bodems prefereren.
Eén gevolg van deze uitkomsten, voor tuiniers in ieder geval, heeft te maken met de stikstof in bacteriën en schimmels. Bedenk dat het bodemvoedselweb voor een plant het volgende betekent: als deze organismen opgegeten worden, dan wordt een deel van de stikstof opgeslagen in het lichaam van de eter, maar veel wordt uitgescheiden in de vorm van het voor de plant beschikbare ammonium (NH4). Afhankelijk van het bodemmilieu kan het ammonium blijven, of het kan omgezet worden in nitriet (NO2) door nitrietbacteriën en daarna in nitraat (NO3) door nitraatbacteriën. Dit proces heet nitrificatie. Wanneer vindt deze omzetting plaats? Als ammonium vrijkomt in bodems die gedomineerd worden door bacteriën. Dergelijke bodems zijn in de regel alkalisch (door het slijm dat bacteriën produceren), waardoor de nitrificerende bacteriën goed gedijen. De zuren die door de schimmels worden uitgescheiden, als ze dominant beginnen te worden, verlagen de pH waardoor dit soort bacteriën sterk in aantal afneemt. In schimmeldominante bodems blijft daardoor een groot deel van de stikstof in ammoniumvorm.
Hier wringt de schoen: kunstmest voorziet de plant wel van stikstof, maar de meeste soorten doen dat – voor minstens de helft –in nitraatvorm. Met wat kennis van het bodemvoedselweb heb je al snel in de gaten dat planten die een voorkeur hebben voor een schimmeldominante bodem niet zullen gedijen op een dieet van nitraten. Met deze kennis ga je je tuin heel anders beheren. Als je schimmels of bacteriën kan laten domineren, of een balans kan krijgen, dan krijgen bepaalde planten de vorm van stikstof die ze het liefst hebben en zullen ze floreren.
Nitrificatie is dus iets anders dan stikstofbinding in wortelknolletjes door bepaalde planten – waarvan sprake was in aflevering 27.

Kunstmest, pesticiden, insecticiden en fungiciden beïnvloeden het bodemvoedselweb, ze zijn giftig voor sommige leden, houden andere op afstand en veranderen het milieu. Belangrijke symbiosen tussen schimmels of bacteriën en planten vinden niet plaats als de planten gratis voedingsstoffen kunnen krijgen. Als planten chemisch gevoed worden, omzeilen ze de door microben gestuurde manier van voedingsstoffen verkrijgen, en microbepopulaties passen zich aan die situatie aan. Het probleem is dus dat je kunstmest moet blijven toevoegen en bestrijdingsmiddelen moet blijven gebruiken omdat de verhoudingen en de diversiteit – de basis van het bodemvoedselweb – verstoord zijn.
Wanneer de bacteriën, schimmels, nematoden en protozoa verdwenen zijn, dan is het logisch dat andere leden van het voedselweb ook verdwijnen. Regenwormen zullen bijvoorbeeld, bij gebrek aan voedsel en geïrriteerd door de synthetische nitraten in wateroplosbare stikstofbemesting, vertrekken. Aangezien zij belangrijke versnipperaars van organisch materiaal zijn is hun afwezigheid een groot verlies. Zonder de activiteit en diversiteit van een gezond voedselweb is niet alleen de voedingsstoffenvoorziening aangetast, maar alle goede dingen die zo’n web met zich meebrengt vallen weg. De bodemstructuur verslechtert, drainage kan een probleem worden, pathogenen en plagen steken de kop op, en: tuinieren en boeren wordt een stuk arbeidsintensiever dan nodig.
Omdat kunstmest op zouten gebaseerd is, vernietigt het gebruik ervan het bodemvoedselweb, voor zover dit nog niet door het frezen (of ploegen) gebeurd is. Dit voorjaarsritueel vernietigt de schimmeldraden, heeft een grote invloed op de wormenpopulatie en verscheurt en verplettert geleedpotigen. Het vernietigt de bodemstructuur en uiteindelijk komt er een tekort aan lucht in de bodem. Ook hier geldt weer dat het je uiteindelijk meer werk kost. Ook luchtvervuiling, pesticiden, fungiciden en herbiciden doden belangrijke leden van de voedselwebgemeenschap, of ‘verjagen’ ze. Elke keten is zo sterk als zijn zwakste schakel: als er een hiaat zit in het bodemvoedselweb, dan stort het systeem in elkaar en zal het niet meer naar behoren functioneren.*
Vanuit de tuinier gezien is het dus zo:
Wie kennis heeft van de werking van bodems en van het bodemvoedselweb kan dat in zijn of haar voordeel, èn in dat van de planten, laten werken. Kunstmest, herbiciden, fungiciden en pesticiden zijn dan niet nodig. Dat scheelt bovendien een hoop werk. Je kunt gedegradeerde bodems verbeteren en ze weer bruikbaar maken. Bodems zullen voedingsstoffen vasthouden in de lichamen van de organismen waardoor ze niet uitspoelen naar het grondwater en de oppervlaktewateren. Je planten zullen de voedingsstoffen krijgen in de vorm die ze willen, en nodig hebben, en zullen minder gestrest zijn. Je zult een natuurlijke ziektepreventie, -bescherming en -onderdrukking verkrijgen. En je bodem zal meer water op kunnen slaan.
De organismen in het bodemvoedselweb zullen het meeste werk doen als het gaat om het gezond houden van je planten. Miljarden levende organismen zullen onvermoeibaar doorwerken, het hele jaar door. Ze doen pittige klusjes, leveren voedingsstoffen aan planten, bouwen beschermende structuren tegen plagen en ziekten, maken de bodem luchtig en verbeteren de drainage, zorgen voor de noodzakelijke doorgangen voor zuurstof en koolstofdioxide. Al die dingen hoef je niet meer zelf te doen.
Tuinieren met het bodemvoedselweb is makkelijk, maar daarvoor moet je het bodemleven terugkrijgen. Een gezond bodemvoedselweb werkt in het voordeel van jou en je planten.’
Hoe je praktisch te werk moet gaan, lees je dus in het boek Het bodemvoedselweb. Daarin worden zelfs de archea behandeld, die men eerst niet zag, en ook niet zocht, want men verwachtte ze eigenlijk alleen in extreme milieus zoals geisers; pas sinds de eeuwwisseling (!) worden ze toch in de bodem gevonden (door genetische herkenning) en hebben ze ‘onze onverdeelde aandacht’ aldus Jeff Lowenfels.
Hiermee eindigt het deel over de bodem en het eerste artikel over de drang van planten en gaan we over naar het tweede artikel dat over de boeren gaat en hun drang.


